Otolaryngologiyhdistyksen
kevätkoulutus
Helsingissä 11. – 12.2.2010
Koulutustilaisuuden teeman oli ”Otology update” ja koulutustilaisuus järjestettiin Scandic Marina Congress Centerissä Katajanokalla. Mukana oli noin 250 otologiasta kiinnostunutta korvalääkäriä. Äkillisen välikorvantulehduksen Käypä hoito ohje on päivitetty ja hyvää päivitystä saimme moneen muuhunkin asiaan. Erityisen mukavaa oli kuulla konduktiivisen kuulovian tutkimuksesta ja biofilmeistä. Paneelikeskustelu oli kerrankin oikeaa keskustelua eikä ulkoa opeteltuja puheenvuoroja. Yleisö lämpeni osallistumaan keskusteluun. Meistä taitaa tulla vähitellen eurooppalaisia! Kaikki muutkin luennot olivat erinomaisia ja innostavia.
Yksi luento ei käsitellyt erikoisalaamme. Filosofi Esa Saarinen lopetti ensimmäisen koulutuspäivän mainioon innostusluentoon. Kapean alan erikoisosaajille se oli keskustelua aiheuttava ja elämää avartava luento. Sen elähdyttävin kohta oli kuvaus maagisen nosteen syntymisestä. Tällainen hetki syntyi Roomassa Zubin Mehtan johtaessa orkesteria ja Placido Domingon esiintyessä solistina. Maaginen noste syntyy tosissaan tekemisestä, haasteesta ja ihmisten välisestä yhteydestä. Me olemme onnellisessa asemassa koska varmaankin jokainen korvalääkäri on saanut kokea tuollaisen hetken leikkaussalissa! Toinen tunnettu suomalainen filosofi, Matti Nykänen on puolestaan todennut: ”Sun pitää antaa tsaanssille mahdollisuus”. Kuinka oikeassa hän onkaan! Iltajuhlassa tunnelmaa nosti kuorosota, hyvä ruoka ja ennen kaikkea hyvä seura.
Harri Saxén
Pneumokokkirokote update
Korvatulehdukseen vaikuttavat rokotteet voivat olla suunnattuja viruksia tai bakteereita vastaan. Influenssa A infektioon assosioitunut välikorvantulehdus vähenee influenssarokotesuojalla 83 %:lla. Influenssakauden aikana rokotteella saadaan 36 %:n vähentyminen välikorvantulehduksiin. Otiiteilla on yhteys rinovirusinfektioihin mutta rinoviruksen variointi on niin suurta, että toistaiseksi rokotetta ei ole odotettavissa. Respiratory syncytial virusta ja parainfluenssavirusta kohtaan tulevaisuus saattaa tarjota rokotteen.
Välikorvantulehduksen aiheuttajabakteeri on useimmiten Pneumokokki, Hemofilus influenzae tai Moraxella. Viimeksi mainitun suhteen rokoterintamalla ei ole liikettä. Kapselillinen hemofilus (tyyppi B) voi aiheuttaa vakavia sairauksia. Sitä vastaan on rokote (Hib), joka on kansallisessa rokotusohjelmassa. Kapseliton hemofilus on puolestaan yleinen korvatulehduksen ja nenän sivuontelotulehduksen aiheuttaja. Hib rokote ei suojaa kapselittoman hemofiluksen aiheuttamilta sairauksilta. Uudessa pneumokokkirokotteessa käytetty D-proteiini saattaa näitä infektioita vähentää.
Markkinoilla on muutama pneumokokkirokote:
Pneumovax polysakkaridirokotteessa on 23 polysakkaridia. Rokote ei toimi pienillä 0-2 vuotiailla lapsilla.
Tarjolla on kaksi konjugaattirokotetta, Prevnar ja Synflorix. Ne ovat immunogeenisia jo alle kolmen kuukauden ikäisillä lapsilla. Ne eivät ole otiittirokotteita. Konjugaattirokotteet ovat melko kalliita (64 – 88 €).
Prevnar on konjugaattirokote, jossa polysakkaridiantigeenit on konjugoitu CRM 197 kantajaproteiiniin. Rokote voi olla seitsemän (PCV7) tai kolmetoista (PCV13) valenttinen. Prevnar rokotuskokeilussa välikorvantulehdukset vähenivät vain 6 %. Viljelypositiiviset otiitit vähenivät 34 % ja rokotetyypin pneumokokin aiheuttamat otiitit vähenivät 57 %. Samaan aikaan kuitenkin ei-rokotetyypin pneumokokkien aiheuttamat otiitit lisääntyivät 31 %. Konjugaattirokote ehkäisee tehokkaasti invasiivisia pneumokokin aiheuttamia tauteja, jotka kuitenkin ovat lapsilla harvinaisia. Yhdysvalloissa se kuuluu yleiseen rokotusohjelmaan ja on luonut myös laumaimmuniteettia.
Se on suunnattu yleisimmin tulehdusta aiheuttavia pneumokokkikantoja kohtaa mutta nyt kuuden vuoden käytön jälkeen maassa on alkanut ilmaantua korvaantumisilmiötä. Infektioita on alkanut aiheuttaa sellaiset pneumokokkikannat, jotka eivät kuulu rokotetyyppiin. Paikoin rokote on jo lähes menettänyt merkityksensä.
Synflorix on kymmenvalenttinen konjugaattirokote (PCV10) ja siinä konjugointiproteiinina on Hemofilus influenzaekannasta saatu D-proteiini. Rokotteen avulla rokoteserotyyppien aiheuttamat korvatulehdukset vähenivät 52 % ja kapselittoman hemofiluksen korvatulehduksissa oli 30 % alenema. Rokotteella on osoitettu myös vaikutus nielukantajuuteen. Rokoteserotyypeissä 42 % vähentyminen ja hemofiluksessa 42 % vähentyminen nielukantajuudessa. Synflorix on sikäli mielenkiintoinen, että sillä on vaikutusta myös kapselittomaan hemofilukseen.
Pneumokokkirokote otetaan suomalaiseen rokoteohjelmaan ilmeisesti syksyllä 2010. Tarjouskilpailu on päättynyt mutta emme tiedä mikä rokote tuli valituksi.
Mitä ehkä tulevaisuudella on tarjota otiittien ehkäisemiseksi:
Pneumokokkia kohtaan saatetaan kehittää proteiinirokotteita.
RSV-parainfluenzaerokote on ehkä mahdollinen.
Rinovirusta kohtaan kehitetään ehkä lääke.
Influenssalääkkeillä voi olla merkitystä otiitin ehkäisyssä.
Bakteerien adheesionestäjät kehittyvät. Ksylitolin käyttö on toistaiseksi ollut hankalaa. Annostelu nenätippoina tai suihkeena voisi sitä helpottaa (Riitta Vertion idea).
Anne Pitkäranta
Äkillinen välikorvantulehdus -
Käypä hoito päivitys
Otiitin käypä hoito ohjeita on kirjoitettu 1999 ja päivitetty aikaisemmin 2004 ja nyt tammikuussa 2010. Uusin päivitys löytyy internetistä http://www.terveysportti.fi/xmedia/extra/hoi/hoi31050.pdf . Ohje on systemaattisesti koottu ja näytön aste luokiteltu (A-D). Ohjeistus on kuvitettu. Tutkimuksen laatu on arvioitu ja sovitettu suomalaiseen järjestelmään. Tässä kuitenkin muutama esityksen huomio viimeisimmistä muutoksista:
Valtaosa otiiteista on bakteerien ja virusten yhdessä aiheuttamia.
Tärkeintä hoidon aloituksessa on kivun hoito.
Luotettava diagnoosi on edellytys antibioottihoidon aloitukselle.
Jos diagnoosi on varma, suositellaan antibioottihoitoa.
Ensisijaiset antibiootit ovat amoksisilliini ja penisilliini.
Mikäli antibioottihoitoa ei aloiteta, lapsi tulisi tutkia 2-3 vrk:n kuluttua, jollei ole selvästi paranemassa.
Kliininen otiitin jälkitarkastus voidaan korvata koulutetun hoitajan tekemällä tympanometriatutkimuksella.
Kitarisan poistolla ei ole merkitystä profylaksiassa.
Otiitin riskitekijät ovat:
altistuminen tupakansavulle (A)
hengitystieinfektio (A)
nuori ikä (A)
päiväkoti- tai perhepäivähoito (A)
perinnöllinen alttius (A)
tutin käyttö (B)
rintaruokinnan puuttuminen tai lyhyt kesto (B)
allergia
Antibiootin hoidon aloittamisen perusteeksi ei riitä se, että tärykalvon takana näkyy eritettä ilman tulehduksen merkkejä. Antibioottihoidosta hyötyy ilmeisesti eniten alle kaksivuotias lapsi, jolla on molemminpuolinen korvatulehdus tai korvan märkävuotoa. Tärykalvopistosta ei ole osoitettu olevan hyötyä paranemiselle.
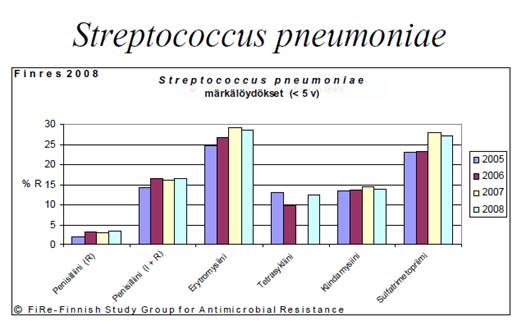
Antibioottien resistenssitilannetta kannattaa seurata. Resistenssitilanteesta löytyy tietoa www.finres.fi
Petri Mattila
Tutkimustietoa antibiooteista lasten äkillisessä välikorvantulehduksessa
Antibioottitutkimukset ovat ongelmallisia koska usein kovin sairaat lapset tippuvat pois tutkimuksista. Onko tutkimustieto yleistettävissä? Erityisesti ongelmallisia ovat voimakasoireiset lapset ja erityisryhmät (Down, halkiolapset, DM1). Voiko tutkimustuloksia yleistää silloinkaan kun verrataan toistuvista otiiteista kärsivää potilasta sporadisiin korvatulehduksiin?
Petri esitteli pari aihetta valaisevaa tutkimusta:
McCormick julkaisi tutkimuksen (Pediatrics 2005) jossa verrattiin vähäoireisen korvatulehduksen paranemista seurannalla ja välittömästi aloitetulla antibioottihoidolla. Antibiooteilla hoidetut lapset paranivat nopeammin mutta antibiootteihin liittyi haittavaikutuksia ja nenänielun bakteerikantajuutta. Hän katsoi, että watchfull waiting sopii näiden korvatulehdusten hoitoon kun huolehditaan oireiden lievittämisestä, vanhempien valistamisesta, jälkiseurannan järjestämisestä ja tarpeen tullen antibiootein tehokkaasti tilanteeseen puuttumisesta.
Watchfull waiting hoidolla tarkoitetaan sitä, että antibioottihoitoa ei aloiteta vaan seurataan tilannetta huolehtien kivun hoidosta ja puututaan tilanteeseen jos korvatulehduksen spontaani paraneminen ei etene odotetulla tavalla. Eri maissa käytännöt vaihtelevat. Alankomaissa antibiootteja on otiitin hoidossa käytetty perinteisesti vähän mutta niiden käyttö on ilmeisesti lisääntymässä.
Rovers julkaisi (Lacet 2006) meta-analyysin, jossa hän katsoi alle kaksivuotiaiden lasten, joilla on molemminpuolinen otiitti tai korvan märkävuoto, hyötyvän eniten antibioottihoidosta.
Leena Hafren
Lasten välikorvantulehduksen perinnöllisyys
Välikorvan tulehdus on yleisin lapsuusajan sairauksista. Se on yleisin syy antibioottihoitoon ja yleisin anestesian syy. Riskitekijät tuli käytyä jo edellisissä esityksessä läpi.
Leena antoi esityksessään lyhyen selvityksen ihmisen genomista, kaksoistutkimusten periaatteista ja single nucleotide polymorfismista (SNP). Näistä asioista keskusteltiin aikaisemmin Otolaryngologiyhdistyksen syyskoulutuksessa 2009.
Kaksoistutkimuksissa on lasten välikorvantulehduksen periytyvyys osoitettu. Norjalaistutkimuksessa oli 4200 lasta ja perinnöllisyydeksi saatiin 70 %. Brittitutkimuksessa perinnöllisyys oli lapsen iästä riippuen 49 – 71 %. Yhdysvaltalaisessa tutkimuksessa välikorvaeritejakson perinnöllisyys oli 73 % ja astman perinnöllisyys 48 – 79 %.
Toistuvat välikorvantulehdukset on yhdistetty geeneihin 10q, 19q, 3p ja 17q.
Nyt Helsingissä tutkitaan 350 perhettä ja yli kahtatuhatta potilasta, joilla on toistuvia otiitteja tai liimakorvatautia. Apuna käytetään kyselylomaketta, kandidaattigeenien selvittämistä ja GWAS-tutkimusta. GWAS (Genomwide association study) sopii yleisten monitekijäisten sairauksien selvittelyyn esim. reuma, ALS, astma, MS, autismi tai statiinien aiheuttama myopatia. Siinä ei tarvita hypoteesia. Ideana on etsiä snippejä, jotka assosioituvat sairauden kanssa. Snippejä voidaan tutkia mikrosirulevyjen avulla.
Geenitutkimus auttaa ymmärtämään sairauden patofysiologiaa ja hoidon oikeaa kohdentamista.
Timo Hirvonen
Huimauspotilaan tutkiminen ja diagnostiikan apuvälineet
Huimaus on yleinen oire, joka lisääntyy iän myötä niin, että 80-vuotiaista 39 % kokee huimaamista. Timo kävi hengästyttävään tahtiin läpi pitkiä listoja erilaisista huimaamista aiheuttavista sairauksista ja niihin liittyvän huimaamisen piirteistä. Pieni terästäytyminen ja esityksen tiukempi kohdentaminen aiheeseen olisi helpottanut maalaislääkäriä hahmottamaan monimutkaista asiaa.
Huimauspotilaan tutkimisessa anamneesin osuus on keskeinen.
ORL-statuksen ja aivohermostatuksen selvittely kuuluu asiaan. Erityisesti tutkitaan silmänliikkeet ja nystagmus. Vestibulospinaalireflekseistä kertoo kehon tasapainon hallinta seistäessä ja käveltäessä.
Kuvantamisen apuvälineenä on TT ja MRI.
TT voi osoittaa yläkaarikäytävän luupuutoksen, dehiskenssin. TT kuvauksella löytyy myös laaja vestibulaarinen aquadukti ja harvinainen jugulaaribulbuksen dehiskenssi, johon voi liittyä laskimopaineen kohoamiseen liittyvää huimausta. Se osoittaa myös kehityshäiriöt, epämuodostumat ja kolesteatoomat.
MRI osoittaa mm. schwannoomat. Tutkimukseen liittyy paljon sivulöydöksiä, joiden kliininen merkitys on kyseenalainen.
Silmänliikkeissä tutkitaan nystagmusta, sakkadeita ja seurantaliikkeitä. Nystagmuksen tutkimiseen kannattaa käyttää Frenzellin laseja. Video-okulografia, VOG soveltuu erinomaisesti kalorisiin kokeisiin ja nystagmuksen analysointiin.
Dix-Hallpiken koe kertoo takakaarikäytävän toiminnasta mutta myös yläkaarikäytävästä. Vaakasuoran kaarikäytävän testaus tehdään selinmakuulla niin, että pää on kallistettu ylöspäin 20º ja kääntäen päätä sivulta toiselle kolmeen kertaan. Suuntaansa vaihtava nystagmus on sentraalista.
Head thrus testissä tutkittavien katseen kuuluisi pysyä tutkijan nenänpäässä kun päätä kierretään sivulle.
Vestibulospinaalirefleksistä kertoo Rombergin koe ja Unterbergerin koe, jossa tutkittava kiertää heikomman korvan suuntaan. Tandemkävely ja Rahkon Walk-rotate-walk testiliittyvät samaan asiaan. Postulografia eli tasapainolevy on epäspesifinen tutkimus.
Otoliittifunktiosta kertoo pään kallistuman määritys. Päällä on taipumus kallistua sairaalle puolelle.
VEMP-tutkimus mittaa esim. klik-ääniärsykkeen aiheuttamia lihaspotentiaalin muutoksia. Päänkäntäjälihas kuvaa sakkuluksen toimintaa ja alasuora silmälihas utrikulusta.
Perifeerisen huimaamisen hoitokeinoissa ei ole uutta tarjolla. Hoidot perustuvat kortisoniin, tasapainoelimen tai hermon tuhoamiseen, asentohoitoihin tai kaarikäytävän tukkimiseen.
Jukka Kokkonen
Huimauspotilas liikenteessä
Liikenteessä näköaisti on dominoiva mutta proprioseptiikka ja vestibulaarisysteemi ovat nekin merkitykselliset.
Liikeaistimukset ovat erityisen tärkeät autoa ajettaessa ja samaan aikaan muuta tehtäessä (esim. autoradion näplääminen). Ne auttavat nopeuden hallinnassa. Niiden häiriö voi aiheuttaa tunteen kaartamisesta, tunteen ohitettavaan törmäämisestä tai tunteen auton kaatumisesta alamäen kaarteessa. Emme lopultakaan oikein osaa sanoa kuinka suuri osa näistä liiketuntemuksista on vestibulaarisia, proprioseptiikkaan liittyviä tai ekstravestibulaarisia (esim. keuhkojen tai sisäelinten liike, verenpaineen muutokset jne.).
Liikennetutkimusta on tehty simulaattorikokeilla. Voidaan tutkia pelkkiä visuaalisia aistimuksia mutta simulaattoreihin voidaan yhdistää myös liikeaistimusten tutkiminen. Liikeaistimukset parantavat suoritusta ja korvaavat näköhavaintoja. Kun annetaan korvaan kalorinen ärsytys, ohjauskäyttäytyminen kaarteissa muuttuu. Kalorinen ärsyke johtaa ajonopeuden hidastumiseen ja taipumukseen ajaa keskiviivan tuntumassa.
Tilastollisesti huimauspotilaat saavat muita harvemmin liikennesakkoja. He eivät aja muita enempää kolareita tai joudu muita useammin poliisin pysähdyttämäksi.
Ei ole näyttöä siitä, että huimaus aiheuttaisi lisääntynyttä riskiä liikenteessä. Riskiä lisää alkoholi, dementia, epilepsia, MS, psykiatrinen häiriö tai skitsofrenia, kaihi ja uniapneatauti tässä järjestyksessä.
Suomessa lääkärillä on ilmoitusvelvollisuus poliisille mikäli terveysvaatimukset eivät täyty ja tila jatkuu yli kahden vuoden ajan. Jatkuvan huimauksen katsotaan olevan este autolla ajoon mutta onko yleensä ottaen jatkuvaa huimausta olemassakaan? Kuorma-autokorttia varten huimauspotilas tarvitsee neurologin lausunnon. Menieren tautia ei pidetä esteenä ajoneuvon kuljettamiselle.
Maailmalla lainsäädäntö vaihtelee kovasti.
Menieren tautia sairastava potilas ei saa ajolupaa Saksassa. Ruotsissa ja Australiassa on ajoluvan rajoituksia ja Britanniassa lupa auton kuljettamiseen tulee vuoden oireettoman jakson jälkeen.
Asentohuimaus ei ole Ruotsissa este autolla ajamiseen. Britanniassa ei ole asiasta ohjeita ja Saksassa se on este ajoluvalle.
Vestibulaarineuriitti on este auton kuljettamiselle Ruotsissa kunnes potilas on toipunut. Saksassa se aiheuttaa ajokiellon.
Loppupäätelmänä on, että näyttöä huimaussairauden aiheuttamasta lisääntyneestä liikenneriskistä ei ole. Suomen lainsäädäntö ei asiaa määritä. Autolla ajon rajoittamiseen huimaussairauden perusteella ei ole tarvetta.
Sirpa Ketola
Huimaukseen liittyvä psykosomatiikka
Aikaisemmin psyyken ja fyysisen terveyden välistä yhteyttä pyrittiin selittämään Alexanderin mallin mukaan. Hyökkäävään luonteeseen katsottiin liittyvän sympatikotonia ja taipumus sairastua mm. reumaan. Vetäytyvään luonteeseen oletettiin liittyvän parasympatikotonian ja separaatioahdistuksen. Nämä altistaisivat teorian mukaan astmalle. Myöhemmin puhuttiin A-tyypin ja B-tyypin ihmisistä. Ensin mainittujen oletettiin olevan alttiita sydänkohtauksille. Tutkimus on kuitenkin osoittanut, että tällaista yhteyttä ei ole.
Nyt ajatellaan, että stressi välittyy elimistöön ja heikoin lenkki sairastuu. Psykiatriakin muuttuu tutkimuksen ja kehittyneen aivoston kuvantamisen myötä. Depressio on todettu itsenäiseksi sydäntaudin riskitekijäksi samalla tavoin kuin verenpainetauti, tupakka ja kohonnut kolesteroli. Ihmisen stressinsiedon katsotaan muodostuvan jo sikiöaikana ja varhaislapsuudessa.
Suhtautumiseemme sairauteen vaikuttaa:
Masentuneisuus
ahdistuneisuus
sosiaalinen verkosto
traumaattiset elämäntapahtumat
tietyt luonteenpiirteet, temperamentti. Tällaisia ovat mm. optimismi/pessimismi, varuillaanolo, impulsiivisuus.
Tahdonvoimalla on merkitystä selviytymisessä. Samanaikainen psyykkinen ja somaattinen sairastaminen lisäävät taakkaa. Psyykkinen oire voi olla somaattisen sairauden syy tai seuraus.
Huimauspotilaista 15 – 57 % on ahdistuneita ja masennusta esiintyy 3 – 15 %:lla. Huimaus, johon liittyy psyykkinen oire aiheuttaa huonon toimintakyvyn ja huonomman ennusteen. Jos potilaalla on aikaisemmin ollut psyykkinen sairaus, somaattinen sairaus voi johtaa psyykkisen sairauden uusiutumiseen.
Vestibulaarimigreeniin liittyy runsaasti psyyken oireita.
Huimauspotilaiden psykiatrinen hoito on samanlaista kuin muidenkin psyykkisten sairauksien hoito. Käyttäytymisterapiasta on hyötyä ja SSRI-lääkkeet ovat keskeisessä asemassa.
Mikael Ojala
Huimaus, kuntoutuminen ja työkyky
Huimaus on oire. Se ei ole diagnoosi tai sairaus, jonka perusteella voisi päästä työkyvyttömyyseläkkeelle. Tarkemmin diagnosoimaton huimaus voi kuitenkin olla peruste lyhyelle SV-jaksolle. Sairauslomaa voidaan tarvita toipumiseen tai tutkimusten ajaksi. Potilaan työ on merkittävä tekijä. Bussikuski, toimistovirkailija ja telineillä kiipeilevä rakennusmies ovat erilaisessa tilanteessa. Diagnostiikkaa on syytä terästää jos potilas ei tunnu toipuvan hyvin. B-lausunto tarvitaan kun sairaus pitkittyy yli kolmen kuukauden. Silloin status on syytä kirjata huolella. Jos statuksessa ei tule erityistä esiin mutta huimaamisoire jatkuu, kannatta etsiä syytä psyykestä tai niskalihastensiosta. Aggravaartio on harvinaista.
Huimauspotilaiden ennuste on hyvä. Heitä pitää aktivoida liikkeelle. Lääkehoidon tulokset ovat vaatimattomia. Alkoholi ja sedatiiviset lääkkeet hidastavat huimauspotilaan toipumista. BPPV on edelleen alidiagnosoitu sairaus.
Työeläkelaissa ei välttämättä tarkastella potilaan työkykyä suhteessa nykyiseen työhön vaan yleiseen työmarkkinoiden työhön. Ammatillista kuntoutusta myönnetään liberaalisti ja työkokeilu on osa tätä kuntoutusta. Maksajana on useimmiten työeläkelaitos, ei KELA.
Työeläkkeelle ei juurikaan mennä kroonisen huimaamisen perusteella. Poikkeuksen tekevät erityisissä töissä olevat iäkkäät potilaat. Työkyvyttömyyseläkkeen syyksi eivät riitä lyhyet kohtaukset (Menieren tauti) tai niiden pelko jos ei ole selvää putoamisen riskiä. Whiplashvamma ei sekään ole työkyvyttömyyden peruste jos mukana ei ole korva-/aivovammaa.
Antti Aarnisalo
Konduktiivisen kuulovian mekanismit, uutta tutkimustyötä
Antti on osallistunut Bostonilaisen työryhmän (Merchant) kuuloluuketjun mekaniikan tutkimukseen. Samankaltaista tutkimustyötä on tehnyt professori Hüttenbrink Dresdenissä. Hänen tutkimuksistaan löytyy referaattia Korvalääkärin kotisivuilta.
Huolellisessa selvittelyssä terveen tärykalvon korvista, joissa oli 20 dB:n gap, löytyi: stapesfiksaatio 68 %:ssa, malleusfiksaatio 2 %, inkuksen fiksaatio 12 %, ketjukatkos, kolmas ikkuna jne.
Laser doppler mittauksella tutkittiin umbon liikkeitä. Mittauksella pystytään erottamaan stapesfiksaatio ja kuuloluuketjun katkos. Tutkittiin myös miten rustosiirteet vaikuttavat tärykalvon värähtelyyn ja äänen johtumiseen.
Optoelektrinen holografia (OEH) mittaa koko tärykalvon liikettä. Samaan aikaa laserdopplerilla mitataan stapeksen liikettä temporaaliluupreparaatissa. OEH muodostaa hologrammin tärykalvon liikkeestä ja auttaa analysoimaan tärykalvon liikkeiden muutoksia eri tilanteissa esim. äänentaajuuden vaihdellessa 500 Hz, 1000 Hz, 4000 Hz tai 8000 Hz.
Tutkimuksissa käytettiin 0,5 mm paksua soikiomaista 6x3 mm rustosiirrettä tärykalvon takana. Testattiin, miten rustosiirre vaikuttaa ollessaan kiinni vapaasti tärykalvossa tai kontaktissa korvakäytävään. Eri äänenpaineilla tärykalvon nanometriliike kyettiin laskemaan. Matalilla taajuuksilla ruston asema ei paljoakaan vaikuttanut. Korkeilla taajuuksilla eroa tuli esiin. Ruston paksuuden merkitys osoittautui vähäiseksi.
Stapeksen liikkeeseen rustosiirre aiheutti pienen muutoksen. Stapeksen liikkeelle ei ollut merkitystä sillä, oliko rusto kiinni korvakäytävän luussa tai ei.
Toisessa koejärjestelyssä preparaatin malleuksen pää tai stapes fiksoitiin luusementillä. Normaaliin verrattuna hologrammin muutokset olivat kovin vähäisiä. Ketjukatkos aiheutti selkeän muutoksen ja stapesfiksaatiokin oli todettavissa.
Tutkimukset antavat potentiaalia uusille kliinisille testeille. Tulevaisuudessa laitteet pienenevät ja tulevat kliiniseen työhön. Postoperatiivisissa tilanteissa tekniikka voisi auttaa kuuloluuproteesin ongelman selvittelyä.
Teemu Kinnari
Biofilmit otologiassa
Bakteeridiagnostiikka perustuu Robert Kochin näkemyksiin. Bakteeri eristetään ja viljellään. Menetelmä antaa tietoa valtapatogeenista mutta pohjimmiltaan kertoo aika vähän. Biofilmien tutkimus alkoi 1960-luvulla ja otolaryngologiaan se tuli 2000-luvun alussa.
Antibioottien teho on huono biofilmibakteereihin. Tarvitaan 100 – 1000 kertaisia antibioottiannoksia. Biofilmi on polymeerimatriksin peittämä inaktiivisessa tilassa oleva bakteeriyhteisö. Biofilmi syntyy bakteerien kohdatessa vihamielisen ympäristön. Bakteereita kiinnittyy pinnalle kun niiden populaatio on riittävä. Alkuun adheesio on reversiibeli mutta muuttuu irreversiibeliksi kemiallisen adheesion myötä. Bakteerien kommunikaation kautta tapahtuu form sensing ja muodostuu sienimäisiä ulokkeita. Niissä voi olla satakerroksinen bakteerimassa. Kypsä biofilmi edustaa latenttia infektiota ja voi pysyä hiljaa jopa vuosia. Aktivaatiossa se päästää bakteereita irti ja voi aiheuttaa akuutin infektion.
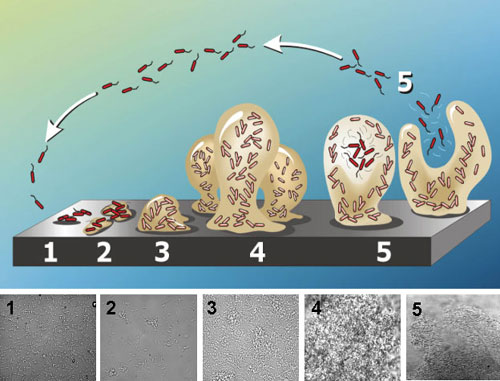
Biofilmin muodostuminen on evoluution kehittämä. Se suojaa bakteereita ympäristön vaikeilta muutoksilta. Luonnon bakteereista 99 % arvioidaan olevan biofilmeissä. Biofilmissä on erilaisen fenotyypin bakteereita. Siinä voi olla useita eri bakteereita ja sieniäkin. Hampaiden plakki on hyvä esimerkki biofilmistä. Suolistossa ja hammasplakissa biofilmit ovat normaaliflooraa mutta 2/3 ihmisen infektioista on biofilmi-infektioita.
Antibioottien teho on tyypillisesti huono. Tyypillistä on myös infektion uusiutuminen lääkekuurin jälkeen ja usein bakteeriviljelynäytteet jäävät negatiivisiksi. Tuntuuko tämä tutulta kun olemme pohtineet toistuvien korvatulehdusten ja OME:n ongelmaa?
Koe-eläintöissä Hemofilus influenzaen muodostama biofilmi näkyy välikorvassa jo vuorokaudessa kokeellisesti aiheutetun otiitin jälkeen. Hall-Stoodley on julkaissut Jamassa 2006 tutkimuksen 26 OME-lapsesta, joista 92 %:lla välikorvasta löytyi biofilmi. Kahdeksan lapsen kontrolliryhmästä sellaista ei löytynyt.
Trakestomiakanyyli, puheproteesi ja tympanostomiaputki on tyypillinen paikka, josta aina löytyy biofilmi. Biofilmi peittää minkä tahansa materiaalin olipa se polyetyleeni, teflon, keraaminen tai timantti. Tämä näkyy hyvin konfokaalimikroskopiassa. Vuoden jälkeen tärykalvoon asennettu titaaniputki on totaalisesti biofilmin peittämä.
Kroonisessa mastoidiitissa antibioottihoito ei auta ja sairaus on vaikeahoitoinen. Kudosnäytteet tuovat esiin biofilmin 5/8 potilaalla.

Ilmari Pyykkö
Nanoteknologiaan perustuva sisäkorvan lääkehoito
on EU-projekti. Sen taustalla on WHO:n tutkimus vuodelta 2002, jossa todetaan
Nanoear on EU-projekti, jonka taustalla on WHO:n raportti vuodelta 2002. Silloin todettiin, että maailmassa on 250 miljoonaa kuulovammasta kärsivää ihmistä. Ongelma lisääntyy tulevaisuudessa kiihtyvää vauhtia. Taustalla on lisääntyvä melualtistus. Ohjelman ja tutkimuksen tavoitteena on kuljettaa nanopartikkeleissa sisäkorvaan lääkkeitä ja geenejä
Jokunen sana mittakaavasta jossa liikutaan. Hiuksen paksuus on 50 000 nm. Punasolun poikkileikkaus on 7000 nm ja bakteerin poikkileikkaus 1000 nm. Virukset ovat 100 nm kokoisia.
Nanopartikkelien koko vaihtelee 3 – 200 nm tasolla. Tässä käytetyt nanopartikkelit:
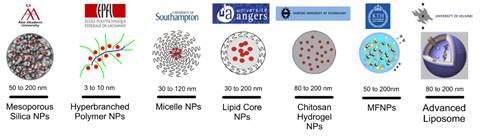
Nanopartikkelit saadaan sisäkorvaan kokleostomian kautta, pyöreän ikkunan läpi tai sisäkorvaistutteen pintamateriaalista.
Linnuilla ulkoiset karvasolut kykenevät uudistumaan. Nisäkkäillä ne eivät kasva mutta sisäkorvassa on prekursorisoluja. Ne ovat kantasolujen seuraava vaihe ja niitä voidaan stimuloida kasvutekijällä. Toivomuksena on saada aikaan toimivia karvasoluja.
Nanopartikkeleihin voidaan liittää:
deksametasoni
BDNF kasvutekijä
geenejä (Atoh-1, BDNF)
siirtäjä RNA
MRI merkkiaine
Nanopartikkeli kulkeutuu solun sisälle ja edelleen tumaan. Sen mukana viety plasmidigeenirengas avautuu ja integroituu solun DNA:han. Tämä johtaa valkuaisaineen tuotantoon.
Nanopartikkelit läpäisevät pyöreän ikkunan. Tutkimuksessa suositaan soluviljelmiä koe-eläinten säästämiseksi. Nanopartikkelit menevät soluihin hyvin viljelmissä mutta huonommin elävässä elimistössä. Elävässä organismissa lysosomi saattaa tuhota nanopartikkeleita ennen kuin ne pääsevät soluihin. Partikkeleita pyritään suojaamaan eräänlaisella susi-lammasten-vaatteissa strategialla.
Toinen keino viedä nanopartikkelit sisäkorvaan on liittää ne sisäkorvaistutteen pintarakenteeseen. Deksametasonilla häiritään fibroblastien lisääntymistä. Seuraavana tavoitteena on kuljettaa kasvutekijä BDNF sisäkorvaan stimuloimaan hermoverkon muodostumista implantin ympärille.
Thomas
Lenarz
Otologian perustutkimuksesta tulevaisuuden diagnostiikkaan ja hoitoon
Professori Lenarz työskentelee Hannoverissa. Lumimyrsky vaikeutti matkaa Helsinkiin mutta luennot saatiin onnellisesti pidettyä.
Kokleaimplantit ovat olleet todellinen menestystarina. Alkuun ne kykenivät luomaan kontaktin ulkomaailmaan. Nyt ne tarjoavat puheen erotuksen lähes kaikille. Häly kuitenkin häiritsee niiden toimintaa. Niiden välittämä informaatio on rajallista. CD levy antaa 700 kbit/s, MP3 soitin 128 kbit/s ja kokleaimplantti 60 – 100 kbit/s.
Kokleaimplanttien toimintaa voidaan parantaa muokkaamalla niiden pintarakennetta, liittämällä nanopartikkeleihin pakattuja lääkeaineita pintamateriaaliin ja stimuloimalla niiden avulla sisäkorvaa optoakustisesti.
Implantin pinnan rakenne vaikuttaa fibroblastien kasvuun ja adheesioon. Fibroblastit vievät tilan hermosolujen dendriiteiltä. Nyt silikonin mikropintarakenteen muokkaaminen ”piikikkääksi” näyttäisi fibroblasteja häiritsevän. Muutos implanttien pintarakenteeseen on odotettavissa lähivuosina. Fibroblasteja voi estää myös polymeeripeitto, josta vapautuu deksametasonia. Lääkkeen vapautuminen on saatava vakioituneeksi ja sen pitoisuuksien on osuttava kapeaan terapeuttiseen ikkunaan. Deksametasonia vapauttavat implantit tulevat markkinoille ehkä jo kolmen vuoden kuluttua.
Nanoear projekti selvittelee mahdollisuutta vapauttaa lääkeaineita implanttiin liitetyistä nanopartikkeleista. Lääkkeen vapautuminen on alkuun kemiallinen tapahtuma mutta sitä voidaan aktivoida myös sähköisesti tai valolla. Tiettyä valon aallonpituutta voidaan antaa esimerkiksi leikkaustilanteessa. BDNF kasvutekijä saattaisi auttaa dendriittejä ympäröimään implantin. Kasvutekijöitä vapauttavat nanopartikkelit tarvitsevat turvallisuustutkimusta. Kasvutekijät tulevat implantteihin yli viiden vuoden päästä.
Sisäkorvan optoakustinen stimulointi on mielenkiintoinen tekniikka. Erotuskyvyn menetystä ei voi kompensoida akustisella vahvistuksella. Tässä tilanteessa ulkoiset karvasolut ovat hävinneet mutta sisäiset jäljellä. Kokleaarinen vahvistus voidaan aikaansaada laserstimulaatiolla. Laserabsorptio lämmittää kudosta, joka laajenee ennen lämmönmenetystä. Syntyy optoakustinen sokkiaalto joka stimuloi paikallisesti sisempiä karvasoluja. Kehitteillä on implantti, jossa on 21 valokuidun kimppu ja valon aallonpituus 530 nm.
Heikki Löppönen
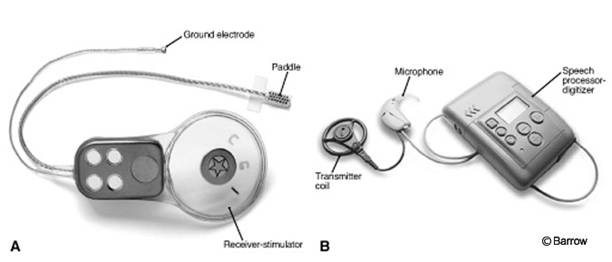
Sisäkorvaistutehoito Suomessa
Suomen ensimmäinen kymmenen implantin sarja asennettiin 1980-luvun puolivälissä Helsingissä. Alku oli hidas mutta toiminta käynnistyi uudelleen vuonna 1995 kun implantit otettiin viiden yliopistosairaalan ohjelmaan. Samana vuonna implantin sai myös ensimmäinen lapsi.
Nyt Suomessa on 636 implanttipotilasta. Aikuisia on 387 ja lapsia 249. Implantteja on asennettu aikuisille 28 / 100 000 ja lapsille 9 / 100 000. Yliopistosairaaloiden toiminnassa on vain pieniä eroja. Hoito on jo rutiinia. Uusia implantteja asennetaan vuosittain 50 – 60. Kuurona syntyviä lapsia on 10 – 15 / vuosi.
Suomessa implanttimarkkinoita johtaa Cochlear ja Med-El on toisena.
Preoperatiivisesti tutkitaan MRI ja TT. Perioperatiivisen TT:n mahdollisuus on käytettävissä. Postoperatiivisia kuvauksia tehdään vain tarvittaessa.
Jussi Jero
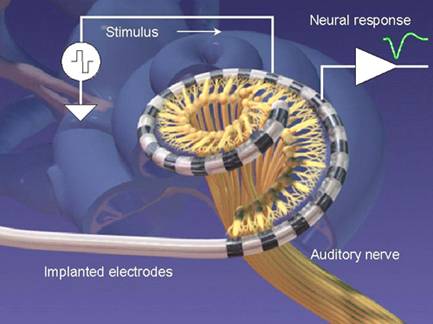
Aivorunkoistute (ABI) Suomessa
Aivorunkoistutteen indikaationa on bilateraalinen akustikusneurinooma (Neurofibromatosis II), bilateraalisesti kuulohermon tuhonnut kallonpohjan murtuma, luutunut koklea tai koklean agenesia. Neurofibromatosispotilaalle ABI voidaan asentaa ns. sleeperiksi, joka aktivoidaan vasta toisenkin korvan kuurouduttua.
House and Hitselberger implantoivat ensimmäisen ABI:n 1979. Nykyisissä implanteissa on 21 elektrodia, jotka pyritään saamaan aivorunkoon kuulotumakkeen tuntumaan.
Leikkaus on teknisesti vaativa, sen kesto vaihtelee viidestä neljääntoista tuntiin. Suomessa ABI on asennettu viidelle potilaalle. Yli 90 %:lla se tukee huuliltalukua ja 85 %:lle se tarjoaa kohtalaisen puheenerotuskyvyn. Vain 5-10 % onnistuu kommunikoimaan puhelimessa. Potilaat ovat onnettoman sairaita ja heille pienenkin avun antaminen tuntuu hyvältä.
Thomas Lenarz
Sensorineuraalisen ja konduktiivisen kuulovian kirurgian uusia tuulia
Kuulokojeet voidaan luokitella:
Akustinen kuulokoje
Elektrinen (Kokleaimplantti, aivorunkoimplantti)
Mekaaninen värähtelijä (BAHA, Sondbridge)
Elektroakustinen hybridi.
BAHA (bone anchored hearing aid) on muuttanut konduktiivisen kuulovian kojehoidon. Se sopii erityisen hyvin käytettäväksi kun luujohtokuulo on bassopäässä kahteen kilohertsiin asti parempi kuin 35 dB. Pienillä lapsilla ongelmana on ohuet luurakenteet. Navigaatiotekniikka helpottaa paksun luun ja oikean ruuvinpaikan löytämistä.
BAHA sopii myös SSD:n (Single sided deafness) hoitoon. Se auttaa äänen suuntimista. Kaikki potilaat eivät sellaista kuitenkaan tahdo kosmeettisten syiden vuoksi.
Välikorvavärähtelijät kilpailevat konventionaalisten kuulokojeiden kanssa. Niiden hinta on kuitenkin korkea. Ne soveltuvat etenkin kroonisen korvakäytävän tulehduksesta kärsivän potilaan kuulokojeeksi ja sekatyyppiseen kuulovikaan.
Vibrant Soundbridge on elektromagneettinen värähtelijä ja se voidaan kiinnittää myös TORP- tai PORP-proteesiin. Se voidaan kiinnittää myös stapeksen levyn läpi vietyyn pistoniin vaikeassa otoskleroosissa tai sovittaa pyöreään ikkunaan. Värähtelijä on osoittautunut luotettavaksi ja niitä on asennettu yli 5000.
Carina on telakkaan kiinnitettävä kokonaan implantoitu värähtelijä, joka liikuttaa inkusta. Sen mikrofoni on ihon alla. Tähän liittyy ongelmana se, että potilas kuulee voimakkaina myös kehonsa omia ääniä (esim. pureskelu). Tämä rajoittaa usein vahvistusta. Laitteen akku vaatii sekin vaihtamista kun se vähitellen muuttuu lataantumattomaksi. Carinalla implantoituja potilaita on runsas 500.
Sisäkorvaistute toimii paremmin jos se saataisiin sijoittumaan modiolaarisesti. Muotoon hakeutuva implantti on suunnitteilla. Puheprosessorit ovat muuttuneet nopeammiksi ja se lisää puheen erotusta. Voidaan myös pyrkiä ohjaamaan virtaa kahden naapurielektrodin välillä amplitudia vaihtaen ja näin tehostaa kuulohermon stimulusta. Implanttien kanavien määrä kasvaa.
Aivorunkoistute lisää tietoisuutta ympäristön äänistä. Se lisää puheen ymmärrystä yhdessä huulioluvun kanssa. Kehitteillä on myös AMI (auditory midbrain implant).
Hybridikuulokojeeseen kuuluu lyhyt elektrodi ja konventionaalinen kuulokoje. Lyhyt elektrodi ei ylety koklean huippuun vaan säästää sen kuulosoluja. Säästynyttä bassopään nurkkakuuloa voidaan tukea konventionaalisella kuulokojeella.
Interetistä löytyy hyvä artikkeli ja erinomaiset kuvat impantoitavista kuulokojeista: Jack Shohet: Implantable hearing devices
Paneelikeskustelu
Ajankohtaista sisäkorvaistutehoidosta
Moderaattorina Heikki Löppönen
Panelistit: Taina Välimaa, Lars Kronlund, Jussi Jero, Erna Tarkiainen, Jukka Kokkonen, Juha-Pekka Vasama
Onko istutehoidon saatavuus Suomessa yhteneväinen?
Kyllä. Kuurousgeeneissä on Suomessa esiintyvyyden vaihtelua ja muuttoliikekin selittää eroja yliopistosairaaloiden välillä. Kriteerit täyttävät saavat kyllä istutteen.
Ei. Ainoastaan Tampereella sovitetaan istute lasten kumpaankin korvaan.
Kaipaavatko indikaatiot muutosta?
Aikuinen saa implantin kun:
Kuulonmenetys on tapahtunut puheen kehittymisen jälkeen
Kuurouden kesto on alle kaksi vuotta
Potilaan kuulovika on bilateraalinen ja vaikea
Kuulokoje ei riitä. Peruste on subjektiivinen ja aktiivisemmin ilmeisesti pitäisi toimia.
Potilas soveltuu leikkaukseen
Potilas sitoutuu kuntoutukseen
Lapsi saa implantin kun:
Ikä on alle 6 vuotta, mieluiten alle 2 vuotta
Bilateraalinen, vaikea kuulovika
Kuulokoje ei riitä
Sisäkorva ja hermo soveltuvat leikkaukseen
Perhe on motivoitunut ja sitoutunut kuntoutukseen
Joissain maissa kuulotestit ovat tarkempia kuin meillä. Tutkitaan puheen erottelua, tavujen erottamista ja hälyn vaikutusta kuuloon. HYKS:ssa edellytetään 50 % tai huonompaa puheenerotuskykyä optimioloissa. Jos kuulokojeesta ei ole riittävää hyötyä, istutteesta on voitava olettaa parempaa hyötyä. Muilla sairauksilla on vaikutusta implanttipotilasta valittaessa. Kuulontutkijoiden pitäisi olla aktiivisia ja osattava löytää mahdolliset implanttikandidaatit kuulokojepotilaistaan. Tässä asiassa tarvitaan lisää koulutusta ja asennetta. Koulutuspäivien yleisö tuntui kaipaavan selkeämpiä kriteereitä, joilla potilas pääsisi yliopistosairaalaan selvityksiin. Joskushan yliopistosairaala voi löytää implantin tilalle optimikuulokojeen.
Toteutuuko lasten universaaliseulonta ja riittääkö se?
Vastasyntyneiltä tutkitaan otoakustiset emissiot tai herätevasteet kattavasti mutta osa kuulovioista kehittyy varhaislapsuudessa. Nyt neuvolatoiminnan alasajo vaarantaa tällaisten lasten löytämisen. Audiometria tehdään neuvoloissa 5-6 vuoden iässä ja kynnysaudiometria koulun alkaessa. Neuvoloissa pyritään kiinnittämään huomiota lapsen puheen kehitykseen mutta epäselvää on, milloin ja miten viivästyneeseen puheenkehitykseen pitäisi puuttua. Yleisön mielestä tämä metodin johtaa diagnoosin viivästymiseen. Terveydenhoitajien pitäisi osata olla herkkiä äidin epäilyksille. Neuvoloiden seulontaa pitäisi lisätä. Vastasyntyneiden universaaliseula saattaa luoda väärää turvallisuudentunnetta siitä, että lapsen kuulo olisi normaali.
Tulisiko istutehoidolle olla yläikäraja?
Vanhusväki on toimintakykyistä. Ikärajoja ei pidä olla. Viime vuonna vanhin HYKS:n istutepotilas oli 79-vuotias mies. Kuurouden kesto ratkaisee. Iällä ei ole merkitystä. Yleisön joukosta ilmoitettiin, että aiheesta on turhaa keskustella. Ikärasismi on laitonta!
Preoperatiiviset tutkimukset – voimmeko olla varmoja, että lapsi on vaikea-asteisesti kuulovikainen?
TAYS:n näkemyksen mukaan aivorunkoaudiometria on riittävä kuulontutkimus. HYKS:ssa on todettu osalla lapsista matalien taajuuksien jäännöskuuloa ja valittu strategiaksi bimodaalikuntoutus. Toiselle puolelle tulee implantti ja toiselle konventionaalinen kuulokoje. Tämä kyseenalaistaa bilateraali-istutehoitoa.
Onko leikkaus turvallinen?
On. Leikkaukseen liittyvät normaalin korvaleikkauksen riskit ja vaara liquorvuodosta ja meningiitista.
Onko laitteissa eroja?
Kilpaa käyvät Cochlear ja Med-El. Niiden hinta on sama. Takuussa tai kestävyydessä ei ole eroja mutta softassa on isoja eroja. Eroa on myös säädettävyydessä ja ulkonäössä. Med-Eliä pidetään teknisesti kehittyneempänä mutta Suomessa niiden revisiotarve on ollut isompi kuin kilpailijalla. Pitkän tähtäimen tuloksissa ei ole eroja.
Pitäisikö lapsille laittaa bilateraali-istute?
Aihe herätti kiivasta väittelyä ja nosti tunteita pintaan. TAYS on Suomessa ainoa yliopistosairaala, jossa lapsille tehdään suoraan bilateraali-istute.
Suomessa on käynnistetty vuonna 2009 HALO-tutkimus molemminpuolisen sisäkorvaistutteen hyödyistä. Kansainvälisen tutkimuksen tuloksia pidetään heterogeenisina. Tutkimusjärjestely tuntuu vaikealta. Miltä tuntuu joutua satunnaistetuksi oman toivomuksen vastaiseen ryhmään?
Maailmalla bilateraalinen istute tuntuu olevan yleinen käytäntö. Niin tehdään Yhdysvalloissa, Ruotsissa, Saksassa ja Britanniassa. Jonkun väittämän mukaan Euroopassa vain Portugal ja Suomi olisivat viimeiset yhden korvan istutteeseen tyytyvät maat. Näin ei kuitenkaan ole.
Istutteiden QALY-hintaa on laskettu:
Lapsella se on unilateraalille implantille 13 000 £
bilateraaliselle implantille 40 000 £
bilateraalille sekventoidulle implantille 54 000 £
Aikuisen QALY-hinta on unilateraalille implantille 14 000£
bilateraaliselle implantille 49 000 £
bilateraaliselle sekvenssoidulle implantille 60 000 £
Yleisö muistutti, että vaikka raha on tärkeää, me olemme kuitenkin lääkäreitä. Lapsella on edessään 80 vuoden elämä. Tämä on eettinen kysymys. Vasta-argumenttina on se, että säästyneellä rahalla voidaan vaikkapa ylläpitää toimivaa neuvolajärjestelmää löytämään kuulovikaiset, kuntoutuksesta hyötyvät lapset ja takaamaan huonokuuloisille hyvä hoito.
Bilateraaliseen implanttiin liittyy ongelmia. Meillä ei ole tietoa siitä, aiheutuuko vanhuudessa ongelmia vestibulaaritoimintaan kun kumpikin korva on implantoitu. Teknisen laitteen tuoma apu on aina rajallista. Emme tiedä onko kummankin korvan implantista oikeasti apua. Sekvensoidusti esim. 1 ja 6 vuoden iässä laitetut istutteet eivät tuo bilateraalisen istutteen etuja. Istutteet tulisi asentaa enintään kahden vuoden välein jos sellainen kumpaankin korvaan halutaan.
Keskustelua olisi mielellään kuunnellut pitempäänkin. Erikoisalaltamme löytyy muitakin väittelyyn innostavia aiheita.

”Sun pitää antaa tsaanssille mahdollisuus”
Takaisin Korvalääkärin kotisivujen sisällysluetteloon
Kuusankoski 22.2.2010
Hannu Tapiovaara