ERS & ISIAN 2006
Tampereella pidettiin 11. – 15. 6. 2006 European Rhinologic Societyn 21. kongressi ja 25. International Symposium on Infection and Allergy of the Nose. Kongressin presidenttinä toimi Markus Rautiainen. Osallistujia oli n. 800. Suurimmat ryhmät tulivat Etelä-Koreasta, Turkista ja Japanista. Suomalaisia osanottajia oli satakunta. Järjestelyt toimivat erinomaisesti ja luentoanti oli hyvä.
Egbert Huizing Alankomaista nosti esiin avajaistilaisuuden puheessaan tärkeän kysymyksen rinologian kielestä, määritelmistä, termeistä ja luokitteluista. Kieleksi on kehittynyt kreikkalaislatinalaisella perustalta nouseva englanninkieli. Terminologia on kuitenkin sekavaa. Nenän ja sivuonteloiden anatomisista rakenteista käytetään useita erilaisia nimiä. Eponyymeistä (esim. Hallerin lokero, Onodin lokero) olisi päästävä eroon. Sivuontelokirurgian termit ovat vieläkin sekavammat. Endoskopia (ESS) kuvaa menetelmää mutta ei kerro mitä leikkauksessa tehtiin. Leikkauksen nimen pitäisi kertoa onko esimerkiksi avattu etummainen seulalokerosto tai tehty antrostomiayhteys poskionteloon. Luokitteluissa olisi luotava tilannetta kuvaava sanallinen järjestelmä. Numerot tai kirjaimet ovat käytännössä hankalia. Kliinikon on vaikea muistaa mitä kasvohermon halvauksen House-Brackmanin luokituksen numerot 1-6, otsaonteloleikkausten tyyppimerkinnät Draf I-III tai tympanogrammin muotoa tarkoittavat kirjaimet A, B ja C tarkoittavat. Kansainvälisesti näitä asioita pohtimaan olisi saatava pysyvä komitea ja julkaistava ”Terminology in Rhinology”.
Luennoilla istuttiin neljän päivän ajan aamusta iltaan. Tähän yhteenvetoon olen kerännyt osan luentoannista. Kaksi luentosarjaa innosti tavallista enemmän ja ne olen merkinnyt pienellä animaatiolla. Kongressi onnistui erinomaisesti. Koulutus oli hintansa arvoista vaikka galaillallisen annista samaa ei voikaan sanoa. Toivon, että yhteenvedostani on iloa kollegoille.
Evidence Based Rhinology
Valerie Lund (UK)


Leonardo da Vinci tutki myös nenän anatomiaa.
Rinologian käsityksiä on muuttanut tietokonetomografia ja Hopkinsin tähystimet. EBM:n pyhänä Graalina on randomoitu kontrolloitu tutkimus. Tutkimus kohdistuu allergiaan, infektioon ja inflammaatioon sekä kasvaimiin. EBM ei kuitenkaan kykene tarjoamaan vastausta kaikkiin kysymyksiin. Tästä on hyvänä esimerkkinä British Medical Journalin kirjoitus jossa etsittiin tieteellistä näyttöä laskuvarjon vaikuttavuudesta lentokoneesta putoavan henkilön hengissä selviämiseen. EBM:n kriteerit täyttäviä tutkimuksia ei löytynyt. Johtopäätelmiä tehtäessä joudutaankin edelleen turvautumaan mielipiteisiin perustuvaan lääketieteeseen ja kliiniseen vaikutelmaan.
Allergisen nuhan hoito on esitetty ARIA-työryhmän julkaisussa. Hoito määrittyy oireen hankaluuden mukaan ja apuna käytetään VAS:a.
Infektion ja inflammaation EBM-yhteenveto on esitetty EPOS3:ssa josta yksinkertaistettu ja lyhennetty versio löytyy osoitteesta Korvalääkärin kotisivut / EPOS 3 . Yhteenvedon kritiikkinä Lund toi esiin:
epäselvän VAS:n
keinotekoisesti määritetyn 12 viikon rajan akuutin ja kroonisen tulehduksen välillä.
Paikallissteroidien hyöty on hyvin osoitettu.
Systeemisesti annostellut steroidit tehoavat myös hyvin kuten kaikki tietävät, mutta niiden tutkiminen ei kiinnosta lääkefirmoja.
Antibiooteista yhtäkään ei ole osoitettu toista paremmaksi.
Makrolidiantibiooteilla on niiden antibakteerisista vaikutuksista riippumaton anti-inflammatorinen vaikutus.
Nenän huuhtelupuhdistuksella on kiistaton teho mutta siihen liittyy edelleen paljon tutkimattomia kysymyksiä.
Sienten vaikutus polyyppitaudin ja kroonisen sinusiitin etiologiaan on edelleen avoin. Nenän amfoterisiinihuuhtelut eivät ole sen tehokkaampia kuin keittosuolahuuhtelut.
Kirurgia selvästi auttaa. Kirurgiankin suhteen tarvitaan paljon tutkimusta. Viiden vuoden seurannassa polypektomian tarjoama helpotus on yhtä hyvä kuin FESS:n teho. Makrolidiantibiootin pitkäkestoisen matala-annoshoidon vaikuttavuus saattaa olla parempi kuin kirurgian.
Radiological Diagnostics in Rhinology
J. Zinreich (USA), M.Fried (USA)
Nenän ja sivuonteloiden kuvantamistutkimuksena natiivikuvien hyöty on vähäinen. TT on muuttunut paljon kahdenkymmenen vuoden aikana. Nykyiset spiraali-TT laitteet ovat nopeita ja ne mahdollistavat laadukkaat rekonstruktiokuvat. Myös 3-D kuvat saadaan spiraalilaitteella vaivattomasti.
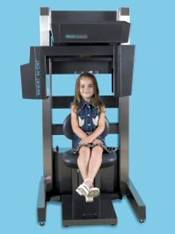
Nyt markkinoille on tullut myös uusi pieni vastaanottohuoneeseen mahtuva TT-laite joka sopii sivuonteloiden kuvantamiseen: Xoran.
Myös MRI-laitteissa on tapahtunut kehitystä. Laitteet mahtuvat jo leikkaussaliin ja niitä käytetään perioperatiivisiin kuvauksiin neurokirurgiassa.
Tavallisen tietokonetomografiaan perustuvan navigaatiolaitteiston tarkkuuden on oltava alle 2mm. Laitteiston käyttö lisää kustannuksia sekä valmistelu- ja leikkausaikaa. Jos laitteistoon tulee toimintahäiriö on osattava selvitä tilanteesta perinteisin keinoin. Tietokoneavusteinen kirurgia sopii:
Revisiokirurgiaan
Kun sinusten anatomia on tavallisesta poikkeava anomalian, aikaisemman kirurgian tai trauman vuoksi.
Kun kyseessä on massiivinen sinonasaalinen polypoosi
Kun patologia käsittää otsaonteloiden, taaempien seulalokeroiden tai kitaontelon alueen.
Tauti liittyy kallonpohjan, orbitan, näköhermon tai carotisvaltimon läheisyyteen
Hoidettaessa endoskooppisesti liquorvuotoa
Benignien ja malignien tuumorien kirurgiaan
Paediatric rhinology
O. Hendley (USA) kertoi lasten rhinovirusinfektioiden olevan hyvin tavallisia. Lapset sairastavat sellaisen kuudesti vuodessa eli yhden rhinovirusinfektion joka toinen kuukausi. Arviolta 50% flunssataudeista on rhinoviruksen aiheuttamia. Rhinoviruksen esiintymishuippu on syksyllä. Rhinoviruksista tunnetaan yli sata serotyyppiä ja eri kantojen välille ei kehity immunologista ristisuojaa. Usein viruksen erittäminen alkaa viikko ennen sairautta ja jatkuu kaksi viikkoa oireiden loppumisen jälkeen.
Lapsen yirusperäinen ylähengitystieinfektio aiheuttaa tavallisesti nenän tukkoisuutta ja yskää kymmenisen vuorokautta. Aivastelu ja nenän vetistäminen lievittyvät alle viikossa. Hengitystieinfektion oireiden huippu on 2 - 4 sairauspäivän kohdalla.
Aila Kristo (FIN) kertasi esityksensä alussa pienen lapsen sivuonteloiden kehityksen. Sivuontelotulehduksen radiologisena kriteerinä pidetään yli 4mm:n limakalvovallia, nestepintaa tai varjostunutta onteloa.
Vuonna 1998 tutkittiin 8 - 9 vuotiaita oululaislapsia sivuonteloiden MRI-kuvantamisella keväällä ja syksyllä. Puolella lapsista todettiin poikkeava löydös. Seuranta-aikana tapahtui muutosta normaalista epänormaaliksi ja päinvastoin.
Vuonna 2003 tehtiin 4 - 7 vuotiaille päiväkotilapsille sivuonteloiden MRI-kuvaus kolmen päivän sisällä hengitystieinfektion alusta. Jos todettiin isoja muutoksia tehtiin kontrollikuvaus kahden viikon kuluttua. Normaali sivuontelolöydös oli vain 12 %:lla ja 68 %:lla todettiin huomattavasti poikkeava löydös. MRI:ssa todetut muutokset korreloivat oireisiin mutta eivät taudin kestoon. Seurantakuvauksessa 69 %:lla oli edelleen yli kolmasosan tilavuuden puutos sivuonteloissa vaikka korjaantumista alkuperäiseen kuvaukseen nähden näkyikin.
Vuonna 2005 tehtiin plasebokontrolloitu kaksoissokkoutettu tutkimus 4 -10 vuotiaiden lasten radiologisesti todetun sivuontelotulehduksen hoidosta kefuroksiimi aksetiililla. Lääkkeellä hoidettujen ja plaseboryhmän välillä ei todettu eroa oireilun paranemisessa tai radiologisen löydöksen normaalistumisessa.
Yhteenveto tutkimustuloksista:
Radiologinen sinusitis on yleinen oireettomilla ja infektiossa olevilla lapsilla
Radiologisesti todettu sinusitis ei ole indikaatio antibioottihoidolle
Ylähengitystieinfektiossa olevat lapset, joilla todetaan röntgenkuvassa varjostuneet sivuontelot, eivät hyödy antibioottihoidosta.
Anne Pitkäranta (FIN) päivitti esityksessään lasten akuutin bakteerisinusiitin hoitoa. Vain 0,5 – 2 % ylähengitystieinfektioista komplisoituu bakteerisinusiitilla. Bakteerisinusiitin katsotaan olevan kyseessä jos oireilu jatkuu 10 – 14 vuorokautta ilman merkkejä paranemisesta. Bakteerisinusiitti on myös silloin kun oireilu on voimakasta (kuume >39 °C, kasvokipu, turvotus kasvojen alueella). Diagnoosi on haasteellinen.
Antibioottihoidon hyödyistä on vain vähän kontrolloituja tutkimuksia. Suomen oloissa suositellaan amoksisilliinia 45 mg / kg / vrk. Lääkeallergisen vaihtoehtona on klaritromysiini. Antibioottihoitoa pitäisi jatkaa 10 – 14 (-28) vrk. Jos antibiootti ei auta 72 tunnin sisällä on syynä väärä diagnoosi tai antibiootille resistentti bakteeri. Tukihoitoon sopivat steroidit, NaCl-pesut, dekongestantit ja antihistamiini.
Toisen vaiheen antibiootiksi (silloin kun ykköslääke ei toimi, lapsella on frontaali- tai sfenoidaalisinusiitti tai komplisoitunut ethmoidaalisinusiitti) suositellaan isoannoksista amoksisilliinia, amoksisilliini-klavulaania tai III polven kefalosporiinia. Komplisoituneen sinusiitin lääkitykseen lisätään usein toiseksi antibiootiksi metronidatsoli.
Maija Hytönen (FIN) kertoi lapsen sinusiitin komplikaatioista. Tavallisesti akuutti rinosinusiitti on hyvänlaatuinen. Pieni osa voi saada komplikaation ja tavallisin on orbitan komplikaatio. Kun lapsella on hengitystieinfektio, päänsärky ja pahoinvointia kannattaa muistaa keskushermoston komplikaation mahdollisuus.
Case Challenges and Nightmares
M Fried, H.P. Dople, D. Kennedy, J. Palmer, Brent Senior ja A. Seiden
Asiantuntijat kävivät stimuloivan paneelikeskustelun. Ongelmia lähestyttiin potilastapausten valossa. Aiheina olivat:
Kasvokipu ilman tai minimaalisilla TT-löydöksillä
Toispuoleinen nenätuumori
Hyvän- ja pahanlaatuiset nenäkasvaimet
Postoperatiivisen epistaxiksen hoito
Spontaani liquorvuoto
Allerginen sienisinusiitti
Frontaalisinusiitti
Osteogeneesi ja krooninen rinosinusiitti
Uusiutuva frontaaliontelon osteooma
Sinonasal Tumours
J. Laranne, H. Iro, P. Koivunen, M. Jorissen, P. Eloy ja P. Douple antoivat selvitystä nenän ja sivuonteloiden pahanlaatuisista kasvaimista.
Lyhyenä yhteenvetona:
Pelkän sädehoidon saaneiden potilaiden ennuste on selvästi huonompi kuin leikkaushoidon saaneiden ennuste.
Postoperatiivinen sädehoito ei näytä vaikuttavan ennusteeseen.
Adenokarsinooman ennuste on hieman parempi kuin levyepiteelisyövän ennuste. Melanooman ennuste on muita syöpätyyppejä huonompi.
Resektion laajuus ja puhtaiden reunojen saavuttaminen leikkauksessa on ennusteen kannalta keskeisen tärkeää.
Tuumorin ulottuminen orbitaan ei sinällään vaikuta ennusteeseen.
Kolmen vuoden kuluttua potilaista on hengissä 51 % ja viiden vuoden kuluttua 39 %.
Seulalokeroston syövän ennuste on parempi kuin poskiontelon syövän ennuste. Jälkimmäinen on usein ehtinyt levinneemmäksi vähäisempien oireidensa vuoksi.
Erityisen huono ennuste liittyy T4b-tuumoreihin jotka ovat levinneet duran tai aivoston alueelle.
Potilailla esiintyy oireilua seitsemän kuukauden aikana ennen kuin diagnoosiin päästään.
Nenän limakalvojen melanooman vartijaimusolmukkeiden tutkimisen merkityksestä ei ole tietoa. Clarke- ja Breslow-luokittelu ei kerro ennusteesta. Melanoomia on vain n. 1 % muutenkin harvinaisista sinonasaalialueen malignoomista.
Nasal and Midfacial Traumatology
R. Mladina, P. Palma, T. Pirilä, R. Kontio
Pietro Palma (Ital) sanoi, että devioiva nenä jossa niin pyramidi, holvi kuin kärkikin ovat vinot, on aloittelijan unelma mutta ekspertin painajainen. Leikkausten tarkoituksena on niin toiminnan kuin estetiikankin parantaminen. Potilaan pitää tiedostaa asymmetria ja hyväksyä, että leikkauksen jälkeenkin asymmetriaa on. Palma esitteli kuvia joissa kasvojen vasen ja oikea puoli oli yhdistetty asymmetrian osoittamiseksi. Paremman mallin puuttuessa askartelin samanlaiset kuvat itsestäni. Ikävää katsottavaa! En tiedä kuka näistä hahmoista vaikuttaa luotettavimmalta. Nenä kuitenkin on niin suora, että siinä ei ole valittamistaJ



Huolellinen nenän analyysi ennen leikkausta on tarpeen. Useita luokitteluja on kehitetty. Kirurgin kannattaa valita itselleen mieluisa, esim:
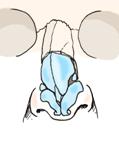
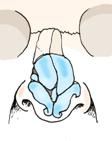
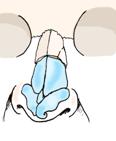
Nenän virheasennon voi ajatella C-kirjaimen tai S-kirjaimen muotoiseksi ja vinoksi kuvien mukaan.
Palma kuvasi esityksessään omaa rinoplastiatekniikkaansa. Yksityiskohtia ei ole tarpeen tässä kuvata tarkemmin.
Tapio Pirilä (FIN) puolestaan kuvasi hitaasti resorboituvien polylaktaattilevyjen käyttöä rinoplastiassa. Palkit ovat 1,5 mm paksuja ja 10 cm pitkiä. Niissä on parikymmentä reikää ja ne ovat muotoiltavissa lämpimässä vedessä vaikka harvoin tätä ominaisuutta tarvitaankaan. Levyn voima säilyy kudoksessa 6 – 12 viikkoa ja levy resorboituu noin kahdessa vuodessa. Levyjä käytetään Spreader strutin tapaan oikaisemaan ja levittämään keskiholvia ja tukemaan nenän selkää kun septum on heikko. Levyt sopivat hyvin käytettäväksi rustosiirteiden kanssa ja ovat hyvin siedettyjä.
Risto Kontion (FIN) esityksen aiheena oli orbitan pohjan murtumat. Orbitan pohjan rekonstruktioon on käytetty erilaisia materiaaleja.
PDS-levy resorboituu liian nopeasti. Luu ei ehdi kasvaa korjaamaan defektiä. Levyn käyttöön liittyy inflammaatiota. Levyä on käytetty pienissä defekteissä joihin liittyy vähäistä herniaatiota. Materiaalia ei pitäisi käyttää orbitan pohjan rekonstruktioon.
PLA-levy resorboituu huomattavasti edellistä hitaammin noin viiden vuoden aikana. Materiaalista on tehty vain vähän kliinisiä tutkimuksia mutta potentiaalisesti se saattaisi sopia pienten defektien hoitoon.
Titanium on stabiili ja helposti muotoiltava materiaali. Sitä käytettäessä ei tarvita luusiirteitä. Titaniumverkosta valmistettu levy sopii orbitamurtumien luudefektin hoitoon. Ongelmana on kuitenkin harvinainen tilanne, jossa levy pitäisi poistaa. Verkkomaisen levyn poisto on vaikeaa. Erityistilanteissa voidaan myös valmistaa yksilöllisesti valettu titaniumlevy.
Luusiirre on kultainen standardi. Sitä on tutkittu paljon ja luukappale on helppo muotoilla. Tavallisin ottokohta on suoliluun harjanteen mediaalilaita. Luusiirre saattaa resorboitua mutta suurempi ongelma on luun ottokohdan kipu. Titaniumverkkoon verrattuna luusiirteen ottaminen on työläs.
Tärkeintä on orbitan pohjan leikkauksissa keskittyä säilyttämään orbitan muoto ja koko. Liukenevia materiaaleja ei pidä käyttää. Luu on luotettava siirre. Titaniumverkko sopii erityisesti pahoihin monimurtumiin.
The Role of Microbes in Chronic Rhinosinusitis (CRS)
N. Otori, R. Kern, S. Lacroix, J. Palmer ja P. Stierna
N. Otori (JAP) pohdiskeli bakteerin roolia kroonisessa rinosinusiitissa. Hän kysyi onko bakteeri ”Leading player or supporting player”?
Kroonisessa rinosinusiitissa polyyppien kanssa luennoitsija katsoi sieni-infektiolla olevan osuutta patogeneesiin. Eosinofiilit ovat tilalle tyypillisiä. Biofilmien, elimistön puolustusjärjestelmän häiriön ja superantigeenien osuus ovat mahdolliset.
Krooniselle bakteriellille rinosinusiitille ovat tyypillistä purulentit eritteet, pysyvä infektio, akuutit pahenemisvaiheet, neutrofiilit ja bakteeri-infektio. Staf. aureuksen exotoksiinit toimivat superantigeeneina. Bakteerientsyymeillä (koagulaasit, proteaasit ja stafylokinaasi) on vaikutusta inflammaatioon.
Japanissa CRS:n bakteeriviljelylöydöksissä:
Staf aureus 26 % Stafylokokkien osuus on nousussa
Hemof. inf. 13,4 % Hemofilus on vähenemässä
Str. pneum. 12,8 % Pneumokokin osuus on pysynyt ennallaan
Mor. catarrh. 5,5 %
Ps. aerug. 5,2 %
Anaer. 1 %
Huomattavassa osassa ei saatu bakteerikasvua esiin lainkaan. Lasten rinosinusiitissa löytyy Japanissakin Staf. aureus vain harvoin. Lapsilla tavallisimmat patogeenit ovat pneumokokki ja hemofilus.
S. Lacroix (SUI) kertoi, että osalla CRS- potilaista löytyy stafylokokkeja limarauhasten solujen, fibroblastien ja nenän epiteelisolujen sisältä. Leikkaushoito ei näitä intrasellulaarisia bakteereita hävitä.
R. Kern (USA) pyrki lähestymään ongelmaa tarkastelemalla enemmänkin kohdetta kuin bakteereita. Superantigeenihypoteesi ja sienihypoteesi ovat vielä kiistanalaisia. Kernin mukaan paikallinen häiriö antigeenien käsittelyssä johtaa CRS:iin.

J. Palmer (USA) kertoi biofilmien olevan itse tuotettuun polymeerimatriksiin sulkeutuneen bakteeriyhteisön, joka voi esiintyä niin kuolleella kuin elävälläkin pinnalla. Biofilmit muistuttavat korallia. Niille on tyypillistä kolonisaatio ja sitä seuraava kasvu. Biofilmien herkkyys antibiooteille on alentunut ja ne pystyvät vastustamaan isännän puolustusmekanismeja. Palmerin mukaan ne pysyvät paikallaan ellei niitä poisteta kirurgisesti. Biofilmejä on todettu lukemattomissa paikoissa, mm. välikorvan tulehduksissa, tympanostomiaputkissa, otsaontelostenteissä ja CRS:ssa. Palmer esitteli upeita elektronimikroskooppikuvia biofilmeistä ja videokuvaa siitä kuinka biofilmit estävät värekarvatoimintaa. Biofilmeistä voi kasvattaa bakteereita.
Vielä ei tiedetä kuinka suurella osalla CRS-potilaista löytyy biofilmi. Emme tiedä kuinka biofilmiä voisi hoitaa ja kuitenkin samalla säilyttää värekarvatoiminnan.
Hyvä yhteenveto löytyy osoitteesta: http://www.genomenewsnetwork.org/articles/06_02/biofilms.shtml
Pontus Stiernan (SWE) aiheena oli steroiditerapian vaikutus bakteereihin CRS:ssa. En löytänyt esityksestä vastausta kysymykseen. Hän pohti sairauden luonnetta. Onko kyse infektiosta vai inflammaatiosta? Paikallinen kudospatologia ilmaantuu päivissä mutta toipuu kuukausia. Limakalvolla kuitenkin on regeneratiivinen taipumus.
Tulehduksen välittäjäaineita tutkimalla on pyritty löytämään eroa CRS:lle ja polyyppitaudille. CRS:lle tyypillisiä ovat TGF-β1, IL-1 α/β, TNFα, IL-6, IL-8 ja IL-3. Polyyppitaudille luonteenomaisia välittäjäaineita ovat IL-5 ja IgE.
Pitäisikö akuutti rinosinusiitti hoitaa antibiootein vai kortikosteroideilla? CRS:ssa kortikosteroidit vaikuttavat Stiernan mukaan ainoilta toimivilta lääkkeiltä.
Viral Rhinology
B. Winther, T. Puhakka, J. Nokso-Koivisto, YJ. Jang ja A. Pitkäranta
Tuomo Puhakka (FIN) puhui nuhakuumeen (Common cold) virusetiologiasta. Nuhakuume on yleisin tulehdustauti ja siinä virukset vaikuttavat niin ylempiin kuin alempiinkin hengitysteihin.
Influenza A – virus eristettiin vuonna 1933. Iso joukko hengitystieviruksia eristettiin1950-luvulla: adenovirus, parainfluenza, rhinovirus, RSV, enterovirus ja coronavirus. Uusia viruksia on eristetty myöhemminkin: torguetenovirus 1997, metapneumovirus 2001, SARS coronavirus 2003, human parechovirus 2006 ja human bocavirus 2006.
Turussa seurattiin vuosina 1995 – 1996 kahdensadan lapsen hengitystieinfektioita ja selvitettiin infektioon liittyviä patogeeneja:
|
Rhinovirus |
52,5 % |
|
Coronavirus |
8,5 % |
|
Influenza A |
5,0 % |
|
Parainfluenza |
3 % |
|
RSV |
2 % |
|
Influenza B |
1,5 % |
|
Adenovirus |
1 % |
|
Kaksoisinfektio |
4,5 % |
|
|
|
|
Chlam. pneumoniae |
2 % |
|
Str. pneum. |
0,5 % |
|
Hemof. infl. |
0,5 % |
|
Mycopl. pneum. |
0,5 % |
|
Morax. catarrh. |
0% |
Taulukon perusteella voi kyllä hyvällä omallatunnolla sanoa nuhakuumeen olevan virusinfektio. Virusinfektio oli kyseessä 69,5 %:ssa sairaustapauksia. Bakteeri löytyi 3,5 %:ssa.
Myöhemmin tehdyissä epidemiologisissa selvittelyissä vinkuvan lapsen hengitystietulehduksen taustalla 95 %:ssa oli virus. Tavallisimmat olivat: Rhinovirus 40 %, RSV 28 %, enterovirus 27 %, bocavirus 19 %, parainfluenza 8 %. Useamman viruksen aiheuttama infektio oli 34 %:lla potilaista.
Johanna Nokso-Koivisto (FIN) kävi läpi hengitysteiden virusinfektion diagnostisia keinoja.
Virusviljely on ollut aikaisemmin kultainen standardi. Tekniikka on työläs ja aikaavievä. Se mahdollistaa elävän viruksen eristämisen
Serologia. Tarvitaan parin viikon välein otettava seerumin näyte ja osoitetaan vasta-aineen tiitterin nousu. Myös serologian ongelmana on hitaus ja se, että testiä ei ole saatavissa kaikille viruksille.
Antigeenien osoitus. Menetelmä on nopea ja herkkä. Se ei vaadi onnistuakseen eläviä viruksia mutta sen sijaan tarvitaan sopiva vasta-aine.
Nukleiinihappojen osoittaminen eli polymerase chain reaction (PCR). Tutkimuksessa monistetaan kohteen DNA-sekvenssi ja se sopii niin RNA- kuin DNA-virustenkin osoittamiseen. Pienikin näytemäärä riittää. Laboratorion kannalta mahdollisen kontaminaation vaara on huomioitava. Multiplex-PCR paljastaa useita viruksia samalla kertaa.
Paras näyte saadaan aspiroimalla limaa nenänielusta. Tämä onnistuu korvalääkäriltä hyvin. Melkein yhtä hyvä näyte saadaan vanupuikolla nenästä. Nielunäyte ei yleensä toimi. Tulevaisuudessa PCR ja antigeenin osoitustutkimukset tulevat lisääntymään. Bedside-testit ovat tulossa.
Antigeenin osoitus on hyvä kun etsitään: Adenovirusta, influenza A ja B, parainfluenzaa ja RSV:aa.
PCR on hyvä etsittäessä: Rhinovirusta, enterovirusta ja influenzaa.
YJ. Jang (Etelä-Korea) kertoi, että perinteisesti ajatellaan virusinfektion aiheuttavan limakalvoturvotusta ja ostiumin tukkeutumisen. Tästä seuraa limakalvon häiriö ja sekundaarinen bakteeri-infektio joka voi johtaa komplikaatioon tai taudin kroonistumiseen. Viruksia (RSV, rhinovirus) onkin todettu akuutin sinusiitin poskionteloeritenäytteissä. Jang pohti ovatko virukset vain sinusiitin ”liipasin” vai ovatko ne aktiivisesti mukana vaikuttamassa tautiprosessiin. Hän tutki CRS-potilaiden nenähuuhtelunäytteiden ja alakuorikosta kyretillä otettujen epiteelisolujen virusnäytteitä. 21 %:lla potilaista löytyi epiteelisoluissa rhinovirus mutta huuhtelunäytteissä virusta ei voitu osoittaa. Kyrettinäyte on tehokkaampi kuin lavaatio nenän virusten osoittamisessa. Viruksen löytyminen voi olla uuden subkliinisen infektion aiheuttamaa ja CRS:n kannalta merkityksetöntä. Toisaalta virukset saattavat olla merkki vanhasta infektiosta ja silloin niiden merkitys CRS:n patogeneesin kannalta jää edelleen avoimeksi.
 Anne
Pitkäranta (FIN) muistutti, että aikaisemmin hengitysteiden
rhinovirusinfektioita ei pidetty pohtimisen arvoisina. Asenne on kuitenkin
muuttumassa.
Anne
Pitkäranta (FIN) muistutti, että aikaisemmin hengitysteiden
rhinovirusinfektioita ei pidetty pohtimisen arvoisina. Asenne on kuitenkin
muuttumassa.
Rhinoviruksen replikaatio tapahtuu nenänielussa ja kitarisassa. Aivastelun, niistämisen ja yskän vaikutuksesta virus leviää nenään, välikorvaan, sivuonteloihin, nielurisoihin, keuhkoputkiin ja keuhkoihin.
Rhinovirusinfektioon liittyy komplikaatioita. OME lasten kitarisassa rhinovirus on usein osoitettavissa samoin kuin akuutin sinusiitin poskionteloiden limakalvollakin. Rhinovirus löytyy pikkulasten toistuvissa respiratorisissa infektioissa bronchuksista. Virus saattaa olla yhteydessä astmaankin. Turvallista ja tehokasta viruslääkettä tarvitaan.
B. Winther (USA) puhui rhinovirusinfektion hoidosta. Tavoitteena on lievittää oireita, estää komplikaatiot, vähentää rhinoviruksen intranasaalista leviämistä ja vähentää tartuttavuutta.
Keinot ovat vähäiset. Echinacae-valmisteita on tutkittu (Turner, NEJM 2005) ja todettu tehottomiksi. NSAID-lääkkeet vähentävät päänsärkyä, yskää ja aivastelua. Intranasaalinen ja systeeminen steroidi näyttävät vähentävän oireita kahden ensimmäisen vuorokauden aikana mutta ne pidentävät viruskylvöä, pitkittävät tautia ja lisäävät lapsilla äkillisen välikorvan tulehduksen riskiä. Paikalliset dekongestantit aukaisevat nenää. Antihistamiinit ja paikallinen ipratropium vähentävät nenän eritystä. Intranasaalinen interferoni tai suun kautta annosteltava pleconaviiri saattavat vähentää komplikaatioriskiä. Hyvä käsihygienia vähentää tarttumisriskiä.
Endoscopic Sinus Surgery
B.S. Gendeh, S. Sütay, C. Yañez
B.S. Gendeh (MAL) Kuinka välttää endoskooppisen sivuontelokirurgian komplikaatioita?
Muista, että shaver voi tehdä erityisesti orbitassa paljon pahaa ennen kuin tajuatkaan.
Harjoitteluvaiheessa pitäisi tehdä sata diagnostista tähystystä ennen kirurgiaan ryhtymistä. Kirurgin alkutaipaleeseen kuuluvat kadaaveriharjoitukset ja leikkaukset supervisorin valvonnassa. Alkuvaiheen leikkaukset voi tehdä porrastetusti. Leikkauspotilaiden seuranta opettaa.
Tee huolelliset preoperatiiviset tutkimukset. Selvitä onko potilaalla vuototaipumus. Leikkaa vasta asiallisen lääkityksen jälkeen. Paikallisesti annosteltavat ja systeemiset steroidit helpottavat työtä. Tarkasta preoperatiivisissa tutkimuksissa potilaan näkö ja dokumentoi löydöksesi.
Tarkasta nenä endoskoopilla ennen kirurgiaa.
Preoperatiiviset TT-kuvat tarvitaan. Jos patologia yltää myös takaethmoidien alueelle, kannattaa pyytää tavanomaisten koronaarileikkeiden lisäksi aksiaalikuvat.
Aloittelevalle kirurgille paikallispuudutustoimenpide on yleisanestesiaa turvallisempi tapa leikata. Luennoitsija kertoi edelleenkin tekevänsä 75 % tähystysleikkauksistaan paikallispuudutuksessa.
Supista limakalvot kokain-adrenalintamponaatiolla ennen toimenpidettä.
Muista, että sivulle katsova skooppi voi johtaa harhaan. Varaa se vain frontaalirekessin hoitoon.
Jos nenässä on paha polyyppitauti tai tehty aikaisemmin kirurgiaa, kannattaa käyttää Wigandin esittelemää tekniikkaa: Lokeroston avaaminen takaa eteenpäin edeten on turvallisinta.
Kiinnitä huomiota etuethmoidien katon alueeseen, orbitan mediaaliseinämään, etu- ja takaethmoidien rajaan ja frontaalirekessiin.
Tavallisimmin komplikaatio kohdistuu orbitaan.
S. Sütay (TUR) puhui leikkauskomplikaatioiden hoidosta. Esitys perustui paljolti leikkausvideoihin.
Surgical Management of Frontal Sinus Disease: Finessing the Options
David Kennedy (USA)
Otsaonteloleikkausten historia on noin sadan vuoden ikäinen. Brieger ja Schonborg esittivät osteoplastisen leikkaustien vuonna 1894. Otsaontelon obliteraation kehitti Hoffmann vuonna 1904. Samana vuonna Killian kuvasi anteriorisen lähestymistien otsaontelon pohjan kautta. Beck suositteli osteoplastiaa ja anteriorista ethmoidektomiaa vuonna 1908. Hän kehotti varomaan luonnollista ostiumia ahtauttavan arpikudoksen vaaran vuoksi. Vuonna 1921 Lynch esitteli frontoethmoidektomian.
Nyt vuonna 2006 Kennedyn mielestä ulkokautta tehtävä frontoetmoidektomia ei enää ole perusteltu. Leikkausten suhteen kannattaa olla konservatiivinen. Endoskooppista leikkausta kannatta koittaa ennen radikaalimpaa kirurgiaa. Obliteraatiota pitää välttää erityisesti jos hoidetaan tuumoria tai allergista sienisinusiittia.
Endoskooppisen otsaontelokirurgian indikaatiot:
Mucocele (erityisesti silloin kun takaseinämässä tai orbitassa on eroosio)
Oireileva krooninen frontaalisinusiitti
Oireileva polypoosi
Mediaalisesti sijaitsevat tuumorit
Akuutti frontaalisinusiitti joka ei vastaa lääkehoitoon
Trauma (otsaontelon seinämän kohottaminen)
Kun frontaalirekessin kirurgiaa suunnitellaan pitää selvittää otsaontelon pneumatisaation aste, otsaontelon drenaasitie, frontaalirekessin koko, mahdollisen uudisluun määrä ja anteriorisen etmoidaaliarterian sijainti. Kuvantamisessa koronaarileikkeet ovat tärkeimmät mutta myös aksiaalileikkeistä tarkastetaan frontaalirekessin alue. Sagittaalisista rekonstruktiokuvista voi myös olla apua alueen anatomian selvittelyssä. Kuvia kannattaa ”skrollata” näytöllä. Tämä auttaa hahmottamaan kolmiulotteista todellisuutta. Kirurgin taito ja myös potilaan halu toteuttaa jälkihoito vaikuttavat onnistumiseen. Frontaalirekessin avaaminen onnistuu parhaiten kun tauti on rajattu. Pitkittynyt tauti johtaa luun paksuuntumiseen ja tämä vaikeuttaa työskentelyä.
Otsaontelon endoskooppiseen kirurgiaan ryhdyttäessä kallonpohja kannattaa identifioida takaa ja edetä sitten anterioriseen suuntaan. Otsaontelo identifioidaan sondin avulla. Jos bulla säästetään intaktina, on vaara jättää supraorbitaalisesti sijaitsevat etmoidilokerot avaamatta. Otsaontelon ostium sijaitsee tavallisimmin prokessus uncinatiuksen keskikuorikon välissä. Luurakenteita murretaan kevyesti sen seudusta ja poistetaan. Tarvitaan kuiva ja veretön työskentelyalue. 45° endoskoopista on huomattavasti apua. Tärkeää on tunnistaa orbitan mediaalilaita ja pysytellä sen tuntumassa.
Kun tehdään ”uncapping the egg” (Draf 2a) käyrästä kyretistä on apua. Limakalvo kannattaa pyrkiä säästämään ja poistamaan luiset ulokkeet. Polyypitkin voi jättää paikalleen jos ostium on vain avoin. Pyritään luomaan halkaisijaltaan yli 4-5 mm:n ostium.

Draf 2b leikkauksessa poistetaan keskikuorikko ja sinuksen avaus ulotetaan keskiviivaan. Se toimii hyvin kun keskikuorikko on osteiittinen tai siitä on kiinnikkeitä orbitan mediaaliseinämään. Otsaontelon on ulotuttava lähelle keskiviivaa. Limakalvo pyritään säästämään erityisesti lateraalisella ja posteriorisella alueella.
Draf 3 leikkauksessa poistetaan nenän septumin yläosa ja otsaonteloita erottava septum. Näin otsaontelot yhdistyvät keskiviivan yli. Leikkausta kutsutaan myös endoskooppiseksi Lothropin leikkaukseksi tai transseptaaliseksi frontaaliseksi sinusotomiaksi. Leikkaus aloitetaan tekemällä Draf 2b leikkaus paremmin identifioitavalle puolelle ja sitten laajentamalla nenän septumin U-muotoisella excisiolla. Navigaatiojärjestelmä auttaa. Otsaonteloon työnnytään poran (70° suojattu timanttipora) tai kyretin avulla. Taakse ei pidä edetä lamina cribriformen etuosaan asti. Toimenpiteen avulla voidaan tehdä revisioleikkaus obliteroituun otsaonteloon ja dreneerata mediaalisesti sijaitsevat mucocelet. Jopa rasvatäytön poisto onnistuu usein ja mahdollistaa ontelon epitelisoitumisen.
Mikä on sitten avoimen osteoplastisen leikkauksen asema? Se on perusteltu eräissä tuumoreissa. Lateraalisesti sijaitseva mucocele tai invertti papillooma jonka poisto ei onnistu endoskooppisesti ovat tavallisimmat syyt avoimeen leikkaukseen. Matalan maligniteettiasteen tuumoreiden hoito on myös syy avoimen osteoplastisen leikkauksen valintaan. Leikkauksessa säästetään terve limakalvo ja onteloa ei tavallisesti obliteroida etenkään silloin kun hoidetaan mucocelea tai potilaalla on allerginen sienisinusiitti. Toimenpide yhdistetään tavallisesti ylhäältä päin tehtävään väljään frontaalirekessin avaamiseen (Lothrop) tai anterioriseen ethmoidektomiaan ja frontaalirekessin dissektioon. Leikkauksen jälkeen väljä näkymä onteloon on mahdollinen. Kirurgian tulokset ovat hyvät ja onnistumisluvut pitkäaikaisseurannassa ovat 75 %:n luokkaa.
Otsaontelon obliteraatiota tarvitaan harvoin. Se voi olla tarpeellinen kun otsaontelo tai frontaalirekessi ovat kovin pienet. Myös silloin kun lähes kaikki limakalvo ontelosta joudutaan uhraamaan, on täyttö tarpeellinen. Erittäin pienissä onteloissa täyttö voidaan toteuttaa poistamalla otsaontelon pohja ja sallimalla orbitan rasvan työntyä onteloon. Limakalvon huolellinen ja täydellinen poisto mikroskooppia apuna käyttäen on olennaisen tärkeää. Yhteys nenään suljetaan faskialla. Kennedyn mielestä rasva on edelleenkin paras ontelon täyttömateriaali. Otsaontelon irrotettu etuseinämä kiinnitetään kahdella pienellä titaanilevyllä. Tavallisimmin toimenpide tehdään bikoronaariviillosta.
Luento oli perusteellinen yhteenveto otsaontelokirurgiasta. Nämä leikkaukset vaativat erityistä perehtyneisyyttä aiheeseen ja myös tarpeeksi isoa sairaalaa, jossa leikkausten määrä on riittävän iso tarjotakseen jatkuvaa harjoitusta. Perusperiaatteena on pyrkiä mahdollisimman konservatiiviseen kirurgiaan. Limakalvoa kannattaa säästää missä se vain on mahdollista. Endoskooppisen toimenpiteen mahdollisuus riippuu niin kirurgin taidoista kuin potilaan anatomiastakin. Draf 2b ja Draf 3 leikkaukset saattavat olla usein hyvä valinta. Osteoplastista obliteraatioleikkausta tarvitaan harvoin.
Endoscopic Sinus Surgery – Evidence of Efficacy
H. Stammberger , V. Lund, H. Brimer
V. Lund (UK) kertoi, että tutkimuksissa endoskooppisen sinuskirurgian tulokset ovat olleet erinomaiset. Paranemista on todettu 80 – 90 %:ssa. Tutkimusten ongelmana on kuitenkin usein vain kolmen kuukauden mittainen seuranta-aika. Paranemisen määritelmä on ongelmallinen samoin kuin kirurgian kuvauskin. Endoskooppisella sinuskirurgialla (ESS) voidaan tarkoittaa erilaisia toimenpiteitä. Leikkaustulokseen vaikuttaa myös taudin vaikeusaste ja muut sairaudet.
Potilaan subjektiivisesti VAS:n avulla arvioimia paranemisen mittareita ovat: Hajuaisti, tukkoisuus, anteriorinen eritys, post nasal drip ja kasvokipu. VAS:ssa kolmen kuukauden makrolidihoidon antama tulos on sama kuin kirurgian tulos! Elämänlaatua mitattaessa kirurgian vaikutus näyttää jatkuvan ainakin 12 kuukauden ajan mutta konservatiivisten hoitojen ja kirurgisen hoidon välillä ei ole eroa!
Objektiivista arviota on pyritty tekemään endoskoopin ja NO-mittausten avulla. Typpioksidi muodostuu sivuonteloissa. Inflammaatio nostaa NO-pitoisuutta. Toisaalta tukkeutuneesta sivuontelosta ei vapaudu lainkaan typpioksidia. Mittaaminen on teknisesti helppoa mutta tulkinta ja mittarin käyttäminen leikkauksen tehon arviossa on hankalaa. Endoskooppikirurgia parantaa objektiivisesti arvioiden myös astmapotilaiden alempien hengitysteiden tilannetta. Lääkehoidon antama teho on kuitenkin tässäkin samanlainen.
Millainen sitten on endoskooppikirurgian vaikuttavuus verrattuna muuhun nenäkirurgiaan? Polyyppien poistoon verrattuna ESS:ssa esiintyy hieman enemmän verenvuotoa mutta hieman vähemmän tarvetta uusintatoimenpiteisiin. Konventionaalisen ethmoidektomian teho on ehkä hieman heikompi kuin tähystysleikkauksen teho. Matti Penttilä on vertaillut tähystyskirurgian vaikuttavuutta Caldwell-Luc leikkaukseen. Lyhyessä seurannassa ESS vaikutti aavistuksen paremmalta mutta pitkäaikaisessa vuosia kestäneessä seurannassa C-L oli parempi vaikka siihen liittyi parestesioitakin.
Hieman mietteliääksi nenäkirurgi tulee kuullessaan lääkehoidon tehon olevan aivan yhtä hyvän kuin kirurgiankin tehon. Vielä mietteliäämmäksi tulee havaitessaan, että eri leikkaustyyppien välistä vaikuttavuuden eroa on vaikea osoittaa.
H.R. Brimer (SUI) totesi hajuaistin häiriön olevan yksi kroonisen rinosinusiitin (CRS) pääoireista. ESS:n vaikuttavuutta hajuaistiin on hankala tutkia. Tulokseen voi vaikuttaa CRS:n alatyyppi, taudin vaikeusaste, hajuaistin mittaamisen vaikeus ja vaikeus selvittää mitä kulloinkin ESS:lla tarkoitetaan. Tähystyskirurgiaa tehdään monella tavalla. Tutkimuspotilaiden valintakin on mutkikasta. Minkä vaikeusasteen potilaita kannattaisi tutkia? Vaikuttaako potilaan käyttämä muu lääkitys tai esim. sairastettu virusinfektio tutkimustulokseen?
ESS:n vaikuttavuutta hajuaistiin on verrattu lääkehoitoon (Blomqvist 2001). Eroa ei ollut! Sinällään leikkaus kyllä vaikuttaa hajuaistiakin parantavasti.
Brimer pohdiskeli voisiko leikkaustekniikalla olla merkitystä hajuaistiin. Usein pyritään medialisoimaan keskikuorikkoa jotta leikkausontelon huolto olisi helpompaa. Kuorikon medialisoiminen kuitenkin kaventaa olfactory cleftia ja heikentää Brimerin mielestä hajuaistia. Hän suosittelee omien tutkimustensa perusteella kuorikon lievää lateralisointia. Stammberger otti kuivakkaan tyylikkäästi kantaa suosittelemalla jättämään kuorikko paikalleen!
RFTA in Rhinosurgery
W. Pirsig, J. Antila, J. Tikanto, M. Gerek, I. Tasca, O. Öðretmenoðlu, Ž. Roje
Jukka Tikanto (FIN) kertoi nenän tukkoisuuden olevan yleinen oire. Syynä on septumdeviaatio, polyypit, allergia tai limakalvoturvotus. Näistä viimeistä on hoidettu monin keinoin. Lääkehoidon lisäksi on käytetty kryohoitoa, kuorikkoresektioita, laseria ja elektrokauterisaatiota. Hoitotoimenpiteisiin on liittynyt sivuvaikutuksia.
Li teki pilottityön alakuorikoiden RFA-hoidosta vuonna 1998. RFA hoidossa kudos lämmitetään 50 – 85 celsiusasteeseen. Toimenpide on turvallinen ja nopea. 80 % potilaista on tyytyväisiä yhden käsittelyn jälkeen viiden kuukauden seurannassa. Tulos on ositettavissa myös nenän tilavuutta mittaavalla akustisella rinometrialla tai vähentyneellä nenäkortikoidin kulutuksella. Hoidon teho arvioidaan nenäkortikoidia paremmaksi mutta hoidon vaikuttavuuden kestosta ei ole tietoa.
M. Gerek (TUR) pohdiskeli kuorsaamista ja obstruktiivista uniapneaoireyhtymää (OSAS). Habituaalista kuorsaamista esiintyy 35 vuotiaista miehistä 20 %:lla ja naisista 5 %:lla. Iän myötä oire yleistyy ja 60 vuotiaista miehistä 60 %:lla ja naisista 40 %:lla esiintyy habituaalista kuorsaamista. Oireeseen vaikuttaa pehmeän suulaen ja uvulan lihastonuksen aleneminen mutta myös alanielun, nenän ja maksillofakiaalisen rakenteen häiriö.
Gerek suositteli RFA:lla tehtävää nielurisojen pienentämistä ja pehmeän suulaen RFA hoitoa. Uvula kannattaa katkaista. Kielen tyven RFA käsittely on kivuliasta ja siihen saattaa liittyä komplikaatioita. Tarvittaessa tehdään alakuorikoiden RFA-hoito. Hyvän hoitotuloksen saavuttamista haittaa jos BMI on >31, potilas tupakoi, käyttää alkoholia tai sedatiiveja.
Myös lapsilla voi esiintyä OSAS ja siihen liittyy kardiovaskulaaristen komplikaatioiden lisääntynyt riski sekä kehityksen, koulunkäynnin ja käytöksen häiriöitä. Tavallisimmat hoitotoimet ovat adenotomia, tonsillektomia, nielurisojen RFA-hoito ja tonsillojen pienentäminen. Lasten nielurisojen pienentämiseen hän suositteli monopolaarislingaa. Nielurisoista kannattaa poistaa 70 %. Sähköslingaamiseen ei liity hänen mukaansa komplikaatioita. Kipu on vähäinen ja lapset palaavat 1-2 vuorokaudessa normaaliaktiviteetteihinsa. Menetelmä ei tietääkseni ole Suomessa käytössä.
 Hot
Water Irrigation in Epistaxis Management
Hot
Water Irrigation in Epistaxis Management
C. Schlegel (SUI)
Tämä luento jäi minulta valitettavasti kuulematta mutta sain paikalla olleilta kollegoilta perusteellisen selvityksen esityksestä. Schlegelin mukaan hankalatkin nenäverenvuodot joita tavallisesti joudutaan hoitamaan potilaan kannalta ongelmallisilla tamponaatioilla tai invasiivisemmilla keinoilla, ovat hallittavissa vuotavan nenäkäytävän kuumavesihuuhteluilla. Hoitomuoto on keksitty jo yli sata vuotta sitten. Näin se käy:
Hyytymät niistetään nenäkäytävästä pois. Vuotava nenäkäytävä puudutetaan 10 %:lla lidokainspraylla tai 4 %:lla tetrakainliuoksella. Adstringoivia aineita ei pidä käyttää. Ballonkikatetrilla suljetaan koaaniaukko. Vuotavaan nenäkäytävään viedään huuhtelukärki johon johdetaan pumpun tai tiputuksen kautta lämmin vesi. Veden lämmön on oltava 50-52 °C. Kuumempi vesi voi aiheuttaa limakalvovauriota. Huuhteluun käytetään 500 ml kuumaa vettä. Parin minuutin vesihuuhtelu voidaan tarvittaessa uusia. Tavallisesti kuitenkin yksi käsittely aiheuttaa limakalvoturvotuksen joka saa vuodon lakkaamaan. Luennoitsija oli kokeillut hoitomuotoa 103:lle posteriorisen vuodon potilaalle. Vain 19:lla hoito ei tuottanut tulosta. Heillä oli tyypillisesti käytössä verihiutaleiden adheesiota estävää lääkitystä. Tässä linkki abstraktiin: Nenäverenvuodon kuumavesihuuhtelu
Hoito on helppo toteuttaa. Se on turvallinen. Nyt kokeilemaan!
Samassa luentosarjassa U. Raghavan (UK) kertoi arteria sfenopalatinan anatomiasta. Nenän takaosan verenvuoto on usein tämän suonen haaroista peräisin. Aikaisemmin nämä vuodot on hoidettu tamponoimalla ja tamponaation pettäessä tarvittaessa poskiontelon kautta tehtävällä a. sfenopalatinan ligeerauksella. Nyt muotiin on tullut radiologin toteuttama embolisaatiohoito. Siihen liittyy riski keskushermoston alueen komplikaatioista mutta myös paikallisten kudosnekroosien vaara. Ongelmaa on myös lähestytty endoskooppisen kirurgian keinoin. Keskikuorikon takapään seudusta etsitään arteria sfenopalatinan haara, joka suljetaan klipsillä tai bipolaaridiatermialla. Tavallisesti tyydytään yhden tai kahden suonihaaran sulkemiseen. Nyt luennoitsija oli analysoinut kymmeniä sfenopalatinavaltimoita. Niille on tyypillistä suuri anatominen variointi. Suurimmassa osassa on enemmän kuin kolme haaraa. Suonihaaroja voi olla kymmenenkin. Tämä on osaltaan hankaloittamassa endoskooppisen hoidon onnistumisen mahdollisuuksia.
The Long Term Macrolide Therapy in CRS
L. Kalogjera, K. Ichimura, V. Lund, A, Cervin, W. Fokkens
L. Kalogjera (CRO) luetteli tutkimukset joiden perusteella pitkäaikaisen makrolidilääkityksen hyödystä on hyvä EBM-näyttö. Emme tiedä miksi makrolidilääkitys toimii kroonisessa rinosinusiitissa. Erilaisia teorioita on esitetty:
Anti-inflammatoorihypoteesi. Makrolidit estävät sytokiinituotantoa (IL-5, IL-88, GM-CSF).
Antimikrobihypoteesi. Antibiootti toimii bakteereita vastaan mutta makrolidilääkitys toimii vaikka bakteerikanta olisi resistentti lääkitykselle.
Quorum sensing – lääkitys saattaa säädellä opportunististen bakteerien virulenssia. Tämä saattaa tapahtua bakteerien väliseen signaaliin tai biofilmin ominaisuuksiin vaikuttamalla.
K. Ichimura (JAP) on makrolidihoidon isä. Lääkityksen käyttämisestä on jo yli kahdenkymmenen vuoden kokemus Japanissa. Kaikki alkoi 1970-luvulla. Diffuusia panbronkioliittia (DPB) sairastanutta potilasta oli hoidettu muutaman vuoden ajan yliopistosairaalassa mutta hoitovaste esim. kortikosteroideille oli erittäin huono. Potilas hävisi kymmeneksi vuodeksi sairaalan kontrolleista kunnes palasi takaisin ja oli yllättäen tautiinsa nähden varsin hyvävointinen. Selvisi, että hän oli käyttänyt kymmenen vuoden ajan erytromysiinilääkitystä 600 mg/vrk. Ichimura oivalsi, että erytromysiinilla täytyy olla joku krooniseen tulehdukseen vaikuttava erityisominaisuus.
CRS:ssa hoitokokeilut aloitettiin vuonna 1990 ja lääkityksen teho oli usein dramaattinen. Hoito alkoi vaikuttaa 2-3 kuukauden sisällä ja lääkkeen teho ei ollut riippuvainen bakteerien antibioottiresistenssistä. Lasten CRS:aan lääkityksen teho ei ollut yhtä hyvä. Massiivi polyyppitauti ja eosinofiilinuha ovat melko resistentit lääkkeen vaikutukselle. Lääkkeen vaikutusmekanismia tutkitaan edelleen. Se näyttää vaikuttavan bakteerien infiltraatioon, nenän värekarvoihin ja eritykseen sekä tulehduksen välittäjäaineiden tuotantoon.

V. Lundin esityksessä pohdittiin matala-annoksisen makrolidihoidon tehon näytön tasoa. Hän myös esitti kysymyksen onko makrolidilääkitys CRS:n hoidossa kirurgiaa parempi hoito.
Vertailevissa prospektiivisissa kokeissa:
VAS-arvioissa lääkkeen teho on vuoden päästä kirurgiaa parempi.
QoL-mittareilla se on yhtä hyvä kuin kirurgialla.
Sakariinin puhdistumamittauksissa ei ole eroa.
Akustisessa rinometriassa lääke on yhtä hyvä kuin kirurgia paitsi silloin kun hoidetaan polyyppitautia.
Endoskooppisessa arvioinnissa ei ollut eroa.
FEV1 mittausten tuloksissa ei ollut eroa.
NO eritys vähentyi lääkkeillä kirurgiaa tehokkaammin
PEF-arvot olivat lääkkein hoidetuilla paremmat
Lääke vaikuttaa niin ylempiin kuin alempiinkin hengitysteihin. Prof. Mygind onkin aikoinaan todennut keuhkojen edustavan posteroinferiorisia seulalokeroita.
Miten makrolidihoito sitten tulisi toteuttaa? Ensinnäkin V. Lundin mielestä aina pitää koittaa maksimilääkehoitoa ennen leikkausta! Makrolidit sopivat ensimmäiseksi lääkkeeksi etenkin erittävän CRS:n hoidossa. Lääkitykseksi sopii hyvin roksitromysiini, klaritromysiini tai erytromysiini mutta annoksena on puolet tavallisesta terapeuttisesta annoksesta. Lääkkeellä tehdään kolmen kuukauden hoitokoe. Jos lääkitys ei lievitä tässä ajassa oireita, sitä ei kannata jatkaa. Jos lääkitys lievittää oireita, voit jatkaa vielä kolmen kuukauden ajan. Myöhemmin oireiden mahdollisesti palatessa aloitetaan hoito uudelleen.
Lääkitys vähentää kirurgian tarvetta. Sitä voi käyttää preoperatiivisesti jolloin se vähentää inflammaatiota ja vuotoa. Lääkitys sopii myös postoperatiiviseen hoitoon tulehdusta vähentävän ominaisuutensa vuoksi.
Lääkityksen teho on eosinofiilisessa riniitissä muuta CRS:aa huonompi. 2,8 % potilaista lopettaa hoidon sivuvaikutusten vuoksi. Tavallisimmat sivuoireet ovat peräisin GI-elimistä. Lähivuosina voimme odottaa lääkitystä käytettävän myös COPD-tautiin, astmaan ja influenzaan. Lääketeollisuus ei ole ollut erityisen kiinnostunut tukemaan tutkimustyötä mutta nyt on saatu käyntiin monikansallinen MACS-tutkimus. Ainakin Japanissa tehdään kokeita makrolidilla, jolla ei ole antibioottivaikutusta mutta anti-inflammatorinen vaikutus on.
Anders Cervin (SWE) on käyttänyt ja tutkinut makrolidilääkkeitä Australiassa. Hän on tutkinut ja käyttänyt lääkitystä niiden potilaiden hoitoon jotka eivät ole saanut helpotusta kirurgisesta hoidosta. Vaikka ESS helpottaakin CRS:aa 85 %:lla jää kuitenkin huomattava joukko potilaista tyytymättömiksi. Cervinin makrolidipotilaat saivat vuoden lääkehoidon. Paraneminen jatkui koko vuoden ajan ja koski päänsärkyoireita, hajuaistia, nenän vuotamista ja potilaan yleistä hyvinvointia. Teho oli osoitettavissa niin VAS-arviossa kuin QoL-mittauksissakin. Vaste lääkitykseen oli parempi niillä potilailla joilla S-IgE oli normaalialueella. Cervin suosittelee makrolidihoitoa sellaisille potilaille joilla:
S-IgE on normaali
on vain lievä allergia
ei ole polyyppeja
steroidien teho on ollut huono
oireena on post nasal drip tai päänsärky
bakteeriviljely on negatiivinen
Cervin on hoitanut joitakin potilaitaan hyvällä menestyksellä jopa 5-6 vuoden makrolidilääkityksellä ilman ongelmia. Se on vaihtoehto kun muut keinot tuntuvat loppuvan. Erittäin tärkeää on kuitenkin muistaa mahdolliset lääkityksen yhteisvaikutukset. Statiinilääkityksen kanssa makrolidit eivät sovi yhteen!
Wytske Fokkens (NL) vahvisti samaa sanomaa kuin muutkin. Lääkkeen tehosta on erittäin vahva EBM-näyttö. EPOS3 paperiin makrolidihoito on sijoitettu varsin varhaiseen vaiheeseen ja sitä suositellaan käytettäväksi jo ennen TT-kuvaustakin.
Dacryocystorhinostomy (DCR) and ORL; Back to Past
H. Tuomilehto, J. Seppä, R. Kamel, M. Bernal-Sprekelsen, M. Önerci
Juha Sepän (FIN) aiheena olivat endonasaaliset DCR-tekniikat. Leikkauksen tavoitteena on saavuttaa tai palauttaa kyynelvuodon toimiminen nenään. Leikkauksella hoidetaan sakkaalisia tai post-sakkaalisia obstruktioita. Obstruktion syy voi olla primaari ja silloin taustalla ovat toistuvat tulehdukset, kroonistunut tulehdus tai kongenitaaliset syyt. Sekundaarisen tukoksen voi aiheuttaa trauma, kirurgia, sädehoito kasvaimet, lähialueen infektiot tai tulehdukselliset sairaudet (esim. Wegener, sarcoidosis).
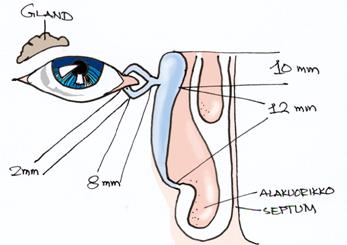
Diagnoosi tehdään tavallisesti sondeeraamalla ja keittosuolahuuhtelulla. Joskus apuna voidaan käyttää fluoreskeiiniväriä, dakryokystografiaa, skintigrafiakartoitusta, TT/MRI kystografiaa ja jopa kanalikulaarista endoskopiaa.
Eksternitietä tehtävän leikkauksen esitteli Toti vuonna 1904. Endonasaalisia tekniikoita ovat esittäneet Caldwell vuonna 1893, West 1911 ja Halle 1914. Myöhemmin endonasaalisiin leikkauksiin on otettu avuksi mikroskooppi, endoskopia, laseravusteinen endoskopia, laseravusteinen transkanalikulaarinen tekniikka ja UÄ-avusteinen endoskopia. YAG-laser on osoittautunut erinomaiseksi apuvälineeksi.
Juha tekee toimenpiteen tavallisesti ohjaamalla valokuidun kanalikkelin kautta helpottamaan pussin paikantamista. Endoskooppia apuna käyttäen tehdään limakalvolappu ja luu aukaistaan joko shaverporalla tai kauhalla. Pussi aukaistaan ja stentataan kyynelpisteiden kautta nenään kulkevalla ohuella silikoniputkella. Joskus tarvitaan lisätoimenpiteenä septoplastiaa, uncinectomiaa tai sinuskirurgiaa.
Jälkihoitoon käytetään steroidi-antibiootti silmätippoja. Systeemiantibioottiin ei ole tarvetta. Nenän huuhteluita keittosuolalla pidetään hyödyllisinä ja noin viikko leikkauksen jälkeen huuhdellaan kyyneltiet ja puhdistetaan leikkausalue. Iäkkäät potilaat hyötyvät keittosuolasilmätipoista. Silikoniputki poistetaan kahden kuukauden kuluttua ja loppukontrolli tehdään puoli vuotta leikkauksen jälkeen. Onnistumisprosentti on 85 %. Juha pohdiskeli voisiko Mitomycin-C olla avuksi revisioleikkauksissa.
Reda Kamel (EGY) kuvasi omaa DCR-tekniikkaansa. Hän ei muodosta limakalvolappua. Osteotomian hän haluaa tehdä pussin alaosaan, johon tehdään pelkkä incisio. Silikoniputkea hän käytti samaan tapaan kuin edellinenkin luennoitsija. Tämän pienen ikkunan tekniikan eduksi hän katsoo paremmin toimivan kyynelpumppujärjestelmän. Silmän räpyttämiseen liittyy aktiivinen kyynelnesteen kuljetus.
M. Bernal-Sprekelsen (SPA) kertoi lasten DCR-leikkauksesta. Synnynnäiset syyt ovat tavallisimmat ja 50 – 70 %:lla kyse on osittaisesta membranoottisesta stenoosista. Näistä 85 % korjaantuu itsestään yhdeksän kuukauden ikään mennessä. Tavallisimmin leikkaus tehdään tarvittaessa parin vuoden ikäiselle lapselle.
Diagnostiikkaan käytetään inspektiota, palpaatiota ja sondeerausta. TT on usein lapsilla hyvä tutkimusapuväline.
Kirurgiassa kapea työskentelytila aiheuttaa omat vaatimuksensa instrumenttien suhteen. Avaus tehdään anteriorisesti. Silikoniputket joutuu usein fiksoimaan ja niitä käytetään 2-3 viikon ajan.
M. Önerci (TUR) antoi hyviä käytännön ohjeita. Hän muistutti, että valokuitu voi ohjata kirurgia liian taakse. Limakalvolapun voi tehdä kanta taaksepäin. Kun ongelma on vanha, siihen liittyy usein luun paksuuntumista. Pussin mediaaliseinä kannattaa excidoida. Silikoniputkea ei aina tarvita. Rinostomian pitäisi olla halkaisijaltaan yli 5 mm:n kokoinen. Postoperatiivisessa vaiheessa tamponeita ei pidä käyttää ja karstoihin ei pidä kajota. Niiden poistaminen tuntuu lisäävän granulointia.
Frontal Sinus Surgery – Endoscopic approach
M. Peltola, H. Moriyama, W. Draf, V. Lund
Matti Peltola (FIN) kertoi otsaontelon täyttöön käytetyistä materiaaleista. Autogeenisista siirteistä tavallisin on rasva. Myös luuta, lihasta ja perikraniaalista kielekettä on käytetty samaan tarkoitukseen. Synteettisiäkin täyttömateriaaleja on kokeilta: akrylaattia, proplastia, kipsiä, hydroksiapatiittia ja nyt uusimpana tulokkaana bioaktiivista lasia S53P4.
Ennen kuin otsaonteloa voidaan täyttää, on kaikki patologia poistettava ja otsaontelo puhdistettava poralla. TYKS:ssa bioaktiivista lasia on käytetty otsaontelon täyttöön 42 potilaan tutkimussarjassa. Bioaktiivisella lasilla täytetyn ontelon jälkiseurantaan ei sovi MRI.

W.Draf (GER) kertoi esityksessään millainen kirurginen lähestymistapa kannattaa missäkin tilanteessa valita. Syvällisempää tietoa on saatavissa hänen oppikirjastaan. Tässä lyhyesti lueteltuna endoskooppiset otsaontelon perusleikkaukset:
Draf I-leikkauksessa avataan etummaiset seulalokerot ja processus uncinatius poistetaan. Näin saadaan frontaalirekessin alue auki. Toimenpide on usein riittävä sivuontelotulehduksen hoitoon.
Draf IIa-leikkauksessa tehdään anteriorisen ethmoidektomian jälkeen sinusotomia esim. kauhaa käyttäen niin, että otsaontelon ostium väljentyy septumista mediaalisesti lamina papyriceaan lateraalisesti.
Draf IIb-leikkauksessa ostiumia väljennetään edelliseen verrattuna poran avulla anterioriseen suuntaan poistamalla otsaontelon pohja sairaalta puolelta mahdollisimman väljästi.
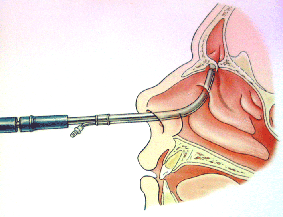
Kuva on peräisin D. Kennedyn esityksestä
Draf III-leikkauksessa poistetaan otsaonteloiden välisen septumin alaosa, nenän septumin yläosa ja otsaonteloiden pohja väljästi lamina papyriceasta toiseen asti.
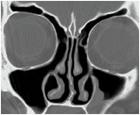
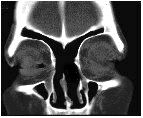

Kuvissa Draf II ja Draf III leikkaukset koronaarileikkeinä. Sagittaalileike Draf IIb-leikkauksesta.
Draf muistutti, että ulkokautta tehtävän otsaonteloleikkauksen ongelmana on vasta vuosia myöhemmin realisoituva mucopyelocele. Joissain tilanteissa kuitenkin ulkoinen bikoronaariviillosta tehtävä leikkaus on perusteltu. Limakalvo on silloin puhdistettava mikroskooppiavusteisesti timanttiporaa käyttäen. Avointa leikkausta kannattaa harkita kun:
otsaontelo on pieni
endonasaalinen leikkaus ei jostain syystä onnistu
otsaontelon takaseinämässä on syöpymä
otsaontelossa on kovin lateraalisesti sijaitseva mucocele.
kyseessä on trauman jälkeinen tulehduksellinen komplikaatio
otsaontelossa on iso osteooma.
Draf suositteli otsaontelon täyttöön rasvakudosta.
V. Lund oli mukana tässäkin istunnossa ja hänen aiheenaan oli Mitomycin C:n merkitys frontonasaalirekessin kirurgiassa. Aine on peräisin streptomyces caespitous-sienestä. Se estää DNA- ja proteiinisynteesiä. Sillä on antibioottisia ominaisuuksia ja se estää fibroblastien toimintaa. Mitomycin C on osoittautunut tehokkaaksi DCR:ssa mutta sen hyödyt endoskooppisessa sivuontelokirurgiassa on vielä epäselvät. Mitomycin C:ta on käytetty otsaontelon endoskooppikirurgiassa estämään ostiumin stenosoitumista. Mitomycin C-liuos (1mg/ml) viedään sideharsotaitteessa käsiteltävälle alueelle ja sen annetaan vaikuttaa viitisen minuuttia. Käsittely voidaan uusia myöhemmin jos ilmaantuu merkkejä re-stenoosista. Toistaiseksi vaikuttaa siltä, että aineesta olisi hyötyä, 86 %:ssa käsitellyistä potilaista väylä on pysynyt avoimena. Polyyppipotilaiden hoidossa aineen tuoma hyöty vaikuttaa heikommalta.
Modern Management of Allergic Rhinitis
Ruby
Pawankar (JAP)
Allergian hoitamisessa tarvitaan näkemystä ja yhteistyötä. Allerginen nuha on astman riskitekijä. 80 %:lla astmaatikoista on allerginen nuha ja toisaalta 40 %:lla nuhapotilaista on astma.
ARIA jaottelee allergisen nuhan näin:
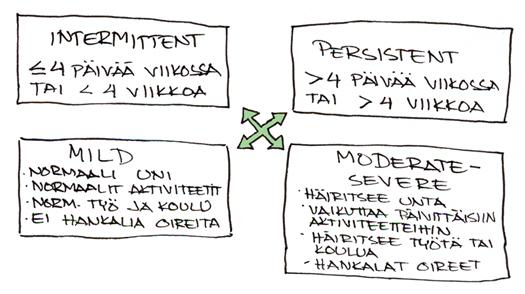
Esitelmöitsijä pohti onko ARIA-työryhmän määritelmä allergisesta nuhasta validi. Kausinuhan ja ympärivuotisen nuhan potilaita menee kumpaankin ryhmään. Kannattaa muistaa, että ”intermittent” ei ole ”seasonal” ja ”persistent” ei ole ”perennial”.
Seasonal nuhan potilaista 20 %:lla on intermittent nuha ja 80 %:lla persistent nuha.
Perennial nuhan potilaista 92 %:lla on persistent nuha ja 8 %:lla intermittent nuha.
ARIA:ssa neuvotaan hoitamaan allergista nuhaa asteittain tehostuvin keinoin http://www.whiar.com/docs/ARIA_PG.pdf . Japanilainen ohje on selkeämpi ja perustuu oireisiin. Valitettavasti ohjetta ei ole saatavissa länsimaisin kirjaimin kirjoitettuna. Allergisen nuhan peruslääkityksenä ovat antihistamiinit ja nenäkortikoidit. Hoitoa suunniteltaessa on otettava huomioon erilaisia tekijöitä. Erityisesti kehitysmaissa kustannukset nousevat tärkeäksi tekijäksi.
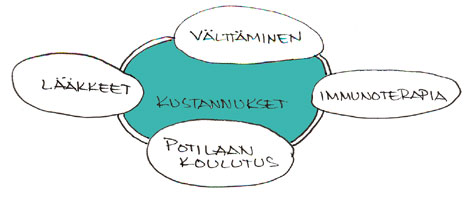
Pawankar kertoi, että ARIA:aan päivitetään anti-IgE ja anti-leukotrieenilääkitykset. Montelukastin avulla voidaan usein puolittaa kalliiden astma-/nenäkortikoidien annos ja saavuttaa säästöä. Immunoterapia on mainittu ARIA-ohjeessa. Se on esitelmöitsijän mielestä kallis ja ongelmallinenkin hoitomuoto. Subkutaanisti annettu hoito näyttäisi kuitenkin estävän astmaa ja myös muiden allergioiden kehittymistä. Sublinguaalisen hoidon tehosta on lisääntyvää näyttöä. Paikallisesti nenään annettavaa spesifistä immunoterapiaa tutkitaan sitäkin.
Epäspesifinen immunoterapia anti-IgE lääkityksellä vähentää kausioireita. Sen on todettu parantavan potilaiden elämänlaatua.
Takaisin Korvalääkärin kotisivuille
Kuusankoskella 7.7.2006
Hannu Tapiovaara